Glosario
O | P | Q | R | S | T | U | V | W | X | Y | Z
-
&
- Útero o Endometrio (Cáncer)
Cáncer que se forma en los tejidos del útero (órgano pequeño, hueco, con forma de pera ubicado en la pelvis de una mujer donde se desarrolla el feto). Los dos tipos de cáncer de útero son el cáncer de endometrio (cáncer que empieza en células que revisten el útero) y el sarcoma uterino (cáncer poco frecuente que empieza en un músculo o en otros tejidos del útero).
El tipo de tumor más frecuente de cáncer de útero es el adenocarcinoma. Se origina en la capa más interna del útero (endometrio).
Otros tipos de tumores son menos frecuentes como el sarcoma, que se origina en la capa muscular del útero o el carcinoma epidermoide, que supone menos de un 1% de todos los tumores del útero.
Para poder determinar el tratamiento más adecuado para el cáncer de útero es importante, tras la intervención quirúrgica, clasificar el tumor, es decir, determinar en qué fase se encuentra.
Estadio I: el cáncer se encuentra localizado en el útero y no afecta a los ganglios linfáticos de la pelvis (esta etapa se puede subdividir en A, B, C dependiendo de la profundidad del tumor en la pared del útero).
Estadio II: el tumor se ha diseminado desde el cuerpo del útero hasta alcanzar el cérvix o cuello del útero.
Estadio III: la lesión alcanza otras estructuras fuera del útero (ovarios, vagina, ganglios de la pelvis) pero permanece confinado a la pelvis.
Estadio IV: el cáncer puede afectar al recto, vejiga y/o ha alcanzado otros órganos más alejados.
Elección del TratamientoUna vez que se ha confirmado el diagnóstico de cáncer de útero y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado para curarla.
El ginecólogo le recomendará y explicará las posibilidades de tratamiento más adecuadas en su caso para que una vez que haya recibido la suficiente información pueda, junto con su médico, tomar una decisión.
El tratamiento del cáncer de útero, como ocurre en la mayoría de los tumores, es un tratamiento multidisciplinar. Distintas especialidades trabajan juntas para combinar terapias y ofrecer a la paciente las mayores posibilidades de curación.
En el tratamiento del cáncer de endometrio se sigue un protocolo, es decir un conjunto de normas y pautas (plan de tratamiento) que se establecen basándose en la experiencia científica para el tratamiento de dicho tumor.
Estos protocolos, que se emplean de forma generalizada en todos los hospitales, recogen las indicaciones o limitaciones de tratamiento en función de una serie de factores:
- Edad de la paciente.
- Tipo de tumor.
- Fase en la que se encuentra la enfermedad.
- El grado de las células.
Probablemente, el médico también tendrá en cuenta si, además del cáncer de endometrio, existen otras enfermedades importantes que puedan dificultar la realización de algún tratamiento específico.
El tratamiento propuesto por el especialista no va a ser el mismo en todas las pacientes.
Los tratamientos más frecuentemente empleados en el cáncer de endometrio son la cirugía, la radioterapia, la hormonoterapia y la quimioterapia.
Cáncer de endometrio en estadio I
El tratamiento del cáncer de endometrio en estadio I puede incluir los siguientes procedimientos:- Cirugía (histerectomía abdominal total y salpingooforectomía bilateral). También se pueden extirpar los ganglios linfáticos de la pelvis y el abdomen para examinarlos bajo un microscopio y verificar la presencia de células cancerosas.
- Cirugía (histerectomía abdominal total y salpingooforectomía bilateral, con remoción de los ganglios linfáticos de la pelvis y el abdomen o sin ella), seguida de radioterapia interna o radioterapia externa dirigida a la pelvis. Después de la cirugía, se puede colocar en la vagina un cilindro plástico que contiene una fuente de radiación para eliminar todas las células cancerosas que queden.
- Radioterapia sola para pacientes que no se pueden someter a cirugía.
Cáncer de endometrio en estadio II
El tratamiento del cáncer de endometrio en estadio II es generalmente una combinación de terapias, incluso radioterapia interna y radioterapia externa y cirugía.
Estadio IIA
El tratamiento del cáncer de endometrio en estadio IIA puede incluir los siguientes procedimientos:
- Cirugía (histerectomía abdominal total y salpingooforectomía bilateral). También se pueden extraer los ganglios linfáticos de la pelvis y el abdomen para examinarlos bajo un microscopio y verificar la presencia de células cancerosas.
- Cirugía (histerectomía abdominal total y salpingooforectomía bilateral, con remoción de ganglios linfáticos de la pelvis y el abdomen o sin esta), seguida de radioterapia interna o radioterapia externa dirigida a la pelvis. Después de la cirugía, se puede colocar en la vagina un cilindro plástico que contiene una fuente de radiación para eliminar todas las células cancerosas que queden.
- Radioterapia sola para pacientes que no se pueden someter a cirugía.
Estadio IIB
El tratamiento del cáncer de endometrio en estadio IIB puede incluir los siguientes procedimientos:
- Cirugía (histerectomía abdominal total y salpingooforectomía bilateral). También se pueden extraer los ganglios linfáticos de la pelvis y el abdomen para examinarlos bajo un microscopio y verificar la presencia de células cancerosas, seguida de radioterapia.
- Radioterapia interna y radioterapia externa, seguida de cirugía (histerectomía y salpingooforectomía bilateral y extirpación de ganglios linfáticos de la pelvis y el abdomen para examinarlos bajo un microscopio y verificar la presencia de células cancerosas).
- Cirugía (histerectomía radical con remoción de los ganglios linfáticos de la pelvis o sin esta, para examinarlos bajo un microscopio y verificar la presencia de células cancerosas).
Cáncer del endometrio en estadio III
El tratamiento del cáncer de endometrio en estadio III puede incluir los siguientes procedimientos:
- Cirugía (histerectomía abdominal total y salpingooforectomía bilateral). También se pueden extraer los ganglios linfáticos de la pelvis y el abdomen para examinarlos bajo un microscopio y verificar la presencia de células cancerosas, seguida de radioterapia interna y radioterapia externa.
- Radioterapia sola para pacientes que no se pueden someter a cirugía.
- Terapia con hormonas para pacientes que no se pueden someter a cirugía o a radioterapia.
Cáncer del endometrio en estadio IV
El tratamiento para el cáncer de endometrio en estadio IV puede incluir los siguientes procedimientos:
- Radioterapia interna y radioterapia externa.
- Terapia con hormonas.
Opciones de tratamiento para el cáncer de endometrio recidivante
El tratamiento del cáncer de endometrio recidivante puede incluir los siguientes procedimientos:- Radioterapia como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida del paciente.
- Terapia con hormonas.
Cirugía
La mayoría de los tumores de endometrio se diagnostican en fases tempranas, es decir, no se han diseminado fuera del útero, por lo que la cirugía suele ser el tratamiento más importante y el primero en llevarse a cabo en la mayoría de estos tumores. Con frecuencia, se añade la radioterapia para completar el tratamiento.
La histerectomía, como la mayoría de las intervenciones quirúrgicas, no está exenta de complicaciones y de efectos adversos, los cuales pueden presentarse con mayor o menor frecuencia tras la intervención. Ésta supone un problema grave para la paciente y altera su calidad de vida.
Cuando se despierte de la anestesia es normal que sienta dolor en la zona de la intervención. Generalmente, el ginecólogo deja pautados fármacos que le aliviarán. Si el dolor no cede, es importante que lo comente con el personal de enfermería o con el médico cuando le visite unas horas después de la cirugía. El dolor, en este caso, no indica problemas de recuperación sino simplemente que hay una herida.
Esta requerirá una serie de cuidados que son similares a los de cualquier cicatriz producida por otra causa. Mientras no se hayan retirado los puntos, el cuidado y limpieza de la misma correrá a cargo del personal sanitario del hospital o del centro de salud. Una vez retirados, es aconsejable mantener una higiene similar a la del resto del cuerpo: lavado diario con agua y jabón.
Una vez que se despierte de la anestesia se mantendrán los sueros hasta que empiece a tolerar los alimentos y líquidos y pueda comenzar una dieta normal.
Es aconsejable que comience a moverse y a caminar pronto una vez que el dolor de la herida quirúrgica sea más tolerable y le permita levantarse, de tal forma que disminuyan los efectos secundarios por inmovilización.
Tras una histerectomía se recomienda no hacer esfuerzos físicos importantes como levantar peso, deportes de contacto o que supongan una sobrecarga muscular de la zona.
Un aspecto importante de la recuperación es el reinicio de la actividad sexual. Generalmente, son necesarias 6-7 semanas para que cicatrice por completo la herida del fondo de la vagina, aunque algunas mujeres pueden requerir más tiempo. Es importante que este tema lo hable con su ginecólogo y le pregunte todas las dudas que le puedan surgir.
Radioterapia
La radioterapia es el empleo de radiaciones ionizantes para el tratamiento, local o locorregional, de determinados tumores que emplea rayos X con altas dosis de irradiación.
Su objetivo es destruir las células tumorales causando el menor daño posible a los tejidos sanos que rodean dicho tumor.
En los tumores de endometrio, la radioterapia que se aplica puede ser externa o interna, aunque generalmente se combinan ambas modalidades.
En la radioterapia externa se emplean equipos generadores de radiación (aceleradores lineales) que en ningún momento contactan con la paciente.
La radioterapia interna consiste en la colocación de materiales radiactivos próximos a la zona tumoral. Se colocan en la cavidad uterina y/o en la vagina, por lo que se denomina radioterapia endocavitaria o intracavitaria.
La radioterapia se puede emplear como tratamiento único, por no poderse practicar cirugía por las condiciones del tumor o de la paciente o tras la cirugía si existen posibilidades de que reaparezca el tumor en la zona donde estaba situado el mismo. Su objetivo en este caso, es destruir las células tumorales que hayan podido quedar tras la cirugía.
El tratamiento con radioterapia siempre es individualizado, es decir, cada enferma tendrá su tratamiento específico y distinto al de otra paciente.
Según la finalidad con que se emplee, la radioterapia puede ser curativa o paliativa para aliviar síntomas provocados por el cáncer de útero tales como dolor, sangrado vaginal, etc.
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como las cabezas femorales, el recto, la vejiga, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..Radioterapia Interna
Es una técnica de tratamiento que consiste en introducir en el interior del organismo isótopos radiactivos. Se pueden implantar de forma temporal o permanente en la zona a tratar.
Con la radioterapia interna se logra administrar altas dosis de radiación a cortas distancias, de tal forma, que llega muy poca dosis a los tejidos sanos circundantes al implante.
¿Cómo se colocan los implantes?Dependiendo del tipo de implante que se vaya a realizar es necesario permanecer ingresado en el hospital durante 1 o dos días, en otros casos el paciente podrá irse a su casa el mismo día tras recibir el tratamiento. Bajo sedación o anestesia general, se efectuará la colocación de los isótopos radiactivos.
¿Es necesario permanecer aislado?En ocasiones, mientras tenga colocados los implantes es necesario que permanezca en una habitación, preparada especialmente para tal fin.
El paciente estará controlado, en todo momento, a través de un monitor de televisión por el personal sanitario responsable de su cuidado.
¿Cuánto dura el tratamiento?La duración del tratamiento dependerá en gran medida del tipo de isótopo que se haya empleado en el implante y de la cantidad de dosis que se quiera administrar en la zona del tumor, pero generalmente oscila entre minutos y días.
-
A
- Ano (Cáncer)
Es el cáncer que se forma en los tejidos del ano. El ano es la abertura del recto (la última parte del intestino grueso) hacia el exterior del cuerpo.
El cáncer del ano es un tumor muy poco frecuente, representando solo el 1,9 % de todos los tumores del tubo digestivo.
Sin embargo en los últimos 10 años esta incidencia ha ido en aumento debido a diferentes factores causantes o etiológicos, como son la infección del virus del Papiloma humano (HPV), de transmisión sexual y la infección por el virus de la inmunodeficiencia humana o SIDA (HIV) y un mayor uso del coito anal, tanto en hombres como en mujeres
El cáncer de ano es un carcinoma epidermoide o escamoso. No existen otras variedades o tipos histológicos.
En cuanto al tamaño, son de mejor pronóstico aquellos tumores menores de 2 centímetros, de pronóstico intermedio los mayores de cinco centímetros y de mal pronóstico los que están invadiendo estructuras vecinas, por ejemplo la vagina o la uretra.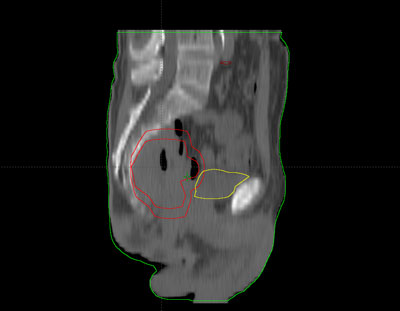
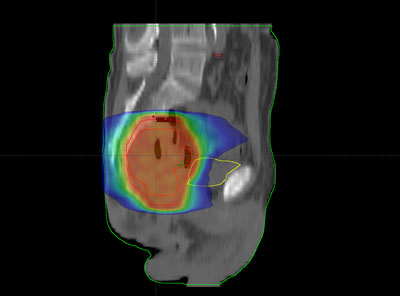
La presencia de metástasis ganglionares y sobre todo la presencia de metástasis viscerales implican un estadio más avanzado.
La clasificación del tumor en estadios se denomina Clasificación TNM y está mundialmente aceptada.
La T se refiere al tamaño del tumor primario:
- Tis: es el tumor “in situ”, confinado a la mucosa, que no traspasa las capas de la misma.
- T1: tumor igual a 2 cm o de menor tamaño (lo tiene el 9 % de los pacientes).
- T2: Tumor entre 2,1cm y 5 cm de tamaño máximo (lo tienen el 51% de los pacientes).
- T3: tumor igual o superior a 5,1 cm. (lo tienen el 30% de los pacientes).
- T4: Tumor de cualquier tamaño pero que invade tejidos de órganos adyacentes, como la uretra, vejiga urinaria o vagina (lo tienen el 10% de los pacientes).
La N se refiere a la presencia o no de afectación de los ganglios linfáticos regionales o más próximos a la zona donde se origina el tumor:- NO significa ausencia de afectación ganglionar.
- N1 significa presencia de afectación tumoral en los ganglios linfáticos perirectales.
- N2 significa metástasis o afectación de la cadena ilíaca interna unilateral o de los ganglios inguinales.
- N3 significa afectación de los ganglios perirectales e inguinales y/o de la cadena ilíaca interna bilateral.
La M se refiere a la presencia confirmada de metástasis a distancia:- MO es ausencia de metástasis.
- M1 es presencia de metástasis a distancia.
Estadio 0 Tis NO MO Estadio I T1 NO MO Estadio II T2
T3
NO
NO
MO
MO
Estadio IIIA T1
T2
T3
T4
N1
N1
N1
N0
MO
MO
MO
MO
Estadio IIIB T4
Cualquier T
Cualquier T
N1
N2
N3
MO
MO
MO
Estadio IV Cualquier T Cualquier N M1 Elección del tratamiento
Dependerá, fundamentalmente, del estadio clínico de la enfermedad tumoral.
De forma resumida se puede decir que los tumores muy localizados (estadios 0 y I) el tratamiento fundamental es la cirugía. Se debe resecar el tumor con un margen de tejido sano periférico de, al menos, 1 cm. Aún así las recurrencias locales son frecuentes (50% de los casos) pero que se pueden tratar de nuevo con cirugía.
Los estadios localmente avanzados (Estadios II y IIIA) deben de tratarse con una combinación de tipos de tratamiento. Lo más recomendable, según los estudios más recientes, es realizar primero un tratamiento con radioterapia y quimioterapia simultáneas (lo que se llama tratamiento quicio-radioterápico neoadyuvante) seguido de una cirugía radical. Las posibilidades de mejorar la supervivencia global son, de este modo, muy significativas.
Los estadio IIIB y IV tienen pocas posibilidades de curación a largo plazo con los tratamientos actualmente conocidos. La quimioterapia y la radioterapia son los tipos de tratamiento más importantes.Cáncer de ano en estadio 0 (carcinoma in situ)
El tratamiento para el estadio 0 suele ser resección local.Cáncer del ano en estadio I
El tratamiento para el cáncer de ano en estadio I puede incluir los siguientes procedimientos:- Resección local.
- Radioterapia de haz externo con quimioterapia o sin ella. Si queda cáncer después del tratamiento, se puede administrar quimioterapia y radioterapia adicionales para evitar la necesidad de una colostomía permanente.
- Radioterapia interna.
- Resección abdominoperineal, si el cáncer permanece o vuelve después del tratamiento con radioterapia y quimioterapia.
- Radioterapia interna para el cáncer que queda después del tratamiento con radioterapia de haz externo.
Los pacientes que han recibido tratamiento para preservar los músculos esfínteres se pueden someter a exámenes de seguimiento cada tres meses durante los primeros dos años, incluso exámenes rectales con endoscopia y biopsia según sea necesario.
Cáncer del ano en estadio II
El tratamiento para el cáncer del ano en estadio II puede incluir los siguientes procedimientos:- Resección local.
- Radioterapia de haz externo con quimioterapia o sin ella. Si queda cáncer después del tratamiento, se puede administrar quimioterapia y radioterapia adicionales para evitar la necesidad de una colostomía permanente.
- Radioterapia interna.
- Resección abdominoperineal, si el cáncer permanece o vuelve después de tratamiento con radioterapia y quimioterapia.
Los pacientes que recibieron tratamiento para preservar los músculos esfínteres se pueden someter a exámenes de seguimiento cada tres meses durante los primeros dos años, incluso exámenes rectales con endoscopia y biopsia según sea necesario.
Cáncer del ano en estadio IIIA
El tratamiento del cáncer de ano en estadio IIIA puede incluir los siguientes procedimientos:
- Radioterapia de haz externo con quimioterapia o sin ella. Si queda cáncer después del tratamiento, se puede administrar quimioterapia y radioterapia adicionales para evitar la necesidad de una colostomía permanente.
- Radioterapia interna.
- Resección abdominoperineal, si el cáncer permanece o vuelve después de tratamiento con radioterapia y quimioterapia.
Cáncer del ano en estadio IIIB
El tratamiento del cáncer de ano en estadio IIIB puede incluir los siguientes procedimientos:- Radioterapia de haz externo con quimioterapia.
- Resección local o resección abdominoperineal, si el cáncer permanece o vuelve después del tratamiento con radioterapia y quimioterapia. Es posible que también se extirpen los ganglios linfáticos.
Cáncer del ano en estadio IV
El tratamiento del cáncer de ano en estadio IV puede incluir los siguientes procedimientos:- Cirugía como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
- Radioterapia como tratamiento paliativo.
- Quimioterapia con radioterapia como tratamiento paliativo.
Opciones de tratamiento para el cáncer de ano recidivante
El tratamiento para el cáncer de ano recidivante puede incluir los siguientes procedimientos:- Radioterapia y quimioterapia para la recidiva después de la cirugía.
- Cirugía, para la recidiva después de la radioterapia o la quimioterapia.
Cirugía
- Resección local: procedimiento quirúrgico en el cual se corta el tumor del ano junto con parte del tejido sano que lo rodea. La resección local se puede utilizar si el cáncer es pequeño y no se diseminó. Con este procedimiento se pueden preservar los músculos esfínteres de manera que el paciente todavía pueda controlar la función intestinal. Los tumores que surgen en la parte inferior del ano se pueden extraer con frecuencia mediante una resección local.
- Resección abdominoperineal: procedimiento quirúrgico por el cual se extirpa el ano, el recto y parte del colon sigmoide a través de una incisión realizada en el abdomen. El médico une el extremo del intestino a una abertura, que se llama estoma, hecha en la superficie del abdomen de manera que los desechos corporales se puedan recoger en una bolsa desechable afuera del cuerpo. Esto se llama colostomía. Los ganglios linfáticos que contienen cáncer también se pueden extirpar durante esta operación.
Quimioterapia
La quimioterapia es un tratamiento para el cáncer que utiliza medicamentos para detener el crecimiento de células cancerosas, ya sea destruyéndolas o impidiendo su multiplicación. Cuando la quimioterapia se toma por vía oral o se inyecta en una vena o en un músculo, los medicamentos entran al torrente sanguíneo y pueden alcanzar las células cancerosas en todo el cuerpo (quimioterapia sistémica). Cuando la quimioterapia se coloca directamente en la columna vertebral, en un órgano o una cavidad corporal como el abdomen, los medicamentos afectan principalmente las células cancerosas de esas áreas (quimioterapia regional). La manera en que se administra la quimioterapia depende del tipo y el estadio del cáncer que se está tratando.
Radiosensibilizador
Los radiosensibilizadores son medicamentos que aumentan la sensibilidad de las células tumorales a la radioterapia. La combinación de radioterapia y radiosensibilizadores puede destruir más células tumorales.
Radioterapia
Su objetivo es destruir las células tumorales causando el menor daño posible a los tejidos sanos que rodean dicho tumor. La radioterapia utiliza energía dirigida a eliminar las células tumorales.
Hay dos tipos de radioterapia. La radioterapia externa utiliza una máquina fuera del cuerpo para enviar radiación hacia el cáncer. La radioterapia interna usa una sustancia radiactiva sellada en agujas, semillas, alambres o catéteres que se colocan directamente adentro del cáncer o cerca de él. La manera en que se administra la radioterapia depende del tipo y del estadio del cáncer que se está tratando.
En los casos de cáncer de ano, la radioterapia permite mantener el ano, en algunos casos si la localización del tumor lo permite aunque también puede producir complicaciones. La quimioterapia concomitante, que permite administrar dosis de radioterapia más bajas y tener menos efectos secundarios. Esta combinación ha demostrado que puede aumentar la supervivencia global y reducir el índice de recaídas.Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como la vejiga, el recto y las cabezas femorales. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control.Radioterapia interna
Es una técnica de tratamiento que consiste en introducir en el interior del organismo isótopos radiactivos. Se pueden implantar de forma temporal o permanente en la zona a tratar.
Con la radioterapia interna se logra administrar altas dosis de radiación a cortas distancias, de tal forma, que llega muy poca dosis a los tejidos sanos circundantes al implante.
¿Cónde se colocan los implantes?
Dependiendo del tipo de implante que se vaya a realizar es necesario permanecer ingresado en el hospital durante 1 o dos días, en otros casos el paciente podrá irse a su casa el mismo día tras recibir el tratamiento. Bajo sedación o anestesia general, se efectuará la colocación de los isótopos radiactivos.
¿Es necesario permanecer aislado?
En ocasiones, mientras tenga colocados los implantes es necesario que permanezca en una habitación, preparada especialmente para tal fin.
El paciente estará controlado, en todo momento, a través de un monitor de televisión por el personal sanitario responsable de su cuidado.
¿Cúanto dura el tratamiento?La duración del tratamiento dependerá en gran medida del tipo de isótopo que se haya empleado en el implante y de la cantidad de dosis que se quiera administrar en la zona del tumor, pero generalmente oscila entre minutos y días.
-
C
- Cévix (Cáncer)
Cáncer que se forma en los tejidos del cuello uterino (el órgano que conecta el útero con la vagina). Por lo general, es un cáncer que crece lentamente, que puede no tener síntomas pero que puede encontrarse con un frotis de Papanicolaou común (un procedimiento en el que se raspan células del cuello uterino y se observan bajo un microscopio). La causa del cáncer de cuello uterino es casi siempre por infección con el virus del papiloma humano (VPH).
Antes del desarrollo definitivo de un cáncer de cérvix, aparecen cambios premalignos en las células, incluso años antes. Estos cambios premalignos pueden denominarse de varias formas: displasia o neoplasia intraepitelial cervical (CIN).
Dependiendo del lugar de origen en el cérvix existen, fundamentalmente, dos tipos de cáncer: el carcinoma epidermoide, derivado de ectocérvix y del fondo de la vagina y el adenocarcinoma. Este último procede de las células del interior del cuello del útero (canal cervical).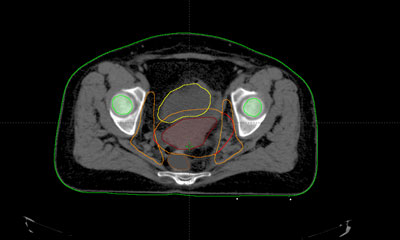
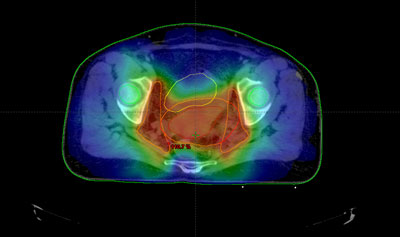
Para poder determinar el tratamiento más adecuado para el cáncer de cuello de útero, es importante "clasificar" el tumor, es decir, determinar en qué fase se encuentra.
Estadio 0: denominado carcinoma in situ o carcinoma preinvasivo. El tumor es muy superficial y se limita a las células de la mucosa.
Estadio I: el tumor está limitado al cuello del útero.
Estadio II: el tumor se ha diseminado fuera del cérvix. Invade la vagina sin llegar al tercio inferior y/o a los ligamentos laterales (parametrios) sin llegar a la pared de la pelvis.
Estadio III: el tumor invade la parte más baja de la vagina, afecta a ganglios linfáticos próximos o alcanza los tejidos laterales del cérvix hasta alcanzar la pared de la pelvis.
Estadio IV: el cáncer se ha extendido a órganos próximos o presenta metástasis.Elección del tratamiento
Una vez que se ha confirmado el diagnóstico de cáncer de cérvix o cuello de útero y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado para curarla. El ginecólogo le recomendará y explicará las posibilidades de tratamiento más adecuadas en su caso, para que una vez que haya recibido la suficiente información pueda, junto con su médico tomar una decisión.
El tratamiento del cáncer de cérvix, como ocurre en la mayoría de los tumores, es un tratamiento multidisciplinar. Distintas especialidades trabajan juntas para combinar terapias y ofrecer a la paciente las mayores posibilidades de curación.
En el tratamiento del cáncer de cérvix se sigue un protocolo, es decir, un conjunto de normas y pautas (plan de tratamiento) que se establecen, basándose en la experiencia científica para el tratamiento de dicho tumor.
Estos protocolos que se emplean de forma generalizada en todos los hospitales, recogen las indicaciones o limitaciones de tratamiento en función de una serie de factores:
- Edad de la paciente
- Fase en la que se encuentra la enfermedad (TNM)
- Deseos de la paciente
Probablemente, el médico también tendrá en cuenta, si además del cáncer de cérvix, existen otras enfermedades importantes que puedan dificultar la realización de algún tratamiento específico.
El tratamiento propuesto por el especialista no va a ser el mismo en todas las pacientes.
Los tratamientos más frecuentemente empleados en el cáncer de cérvix son la cirugía, la radioterapia y la quimioterapia.Estadio 0 (carcinoma in situ)
El tratamiento del estadio 0 puede incluir los siguientes procedimientos:
- Procedimiento de escisión electroquirúrgica con asa (LEEP).
- Cirugía láser.
- Conización.
- Criocirugía.
- Histerectomía total, en el caso de mujeres que no pueden o que no desean tener hijos.
- Radioterapia interna, en el caso de mujeres que no se pueden someter a una cirugía.
Cáncer de cuello uterino en estadio IA
El tratamiento del cáncer de cuello uterino en estadio IA puede incluir los siguientes procedimientos:- Histerectomía total, con salpingooforectomía bilateral o sin esta.
- Conización.
- Histerectomía radical modificada y extirpación de ganglios linfáticos.
- Radioterapia interna.
Cáncer de cuello uterino en estadio IB
El tratamiento del cáncer de cuello uterino en estadio IB puede incluir los siguientes procedimientos:- Combinación de radioterapia interna y radioterapia externa.
- Histerectomía radical y extirpación de ganglios linfáticos.
- Histerectomía radical y extirpación de los ganglios linfáticos, seguidas de radioterapia más quimioterapia.
- Radioterapia más quimioterapia.
Cáncer de cuello uterino en estadio IIA
El tratamiento del cáncer de cuello uterino en estadio IIA puede incluir los siguientes procedimientos:- Combinación de radioterapia interna y radioterapia externa, más quimioterapia.
- Histerectomía radical y extirpación de ganglios linfáticos.
- Histerectomía radical y extirpación de los ganglios linfáticos, seguidas de radioterapia más quimioterapia.
Cáncer de cuello uterino en estadio IIB
El tratamiento del cáncer de cuello uterino en estadio IIB puede incluir radioterapia interna y radioterapia externa, combinada con quimioterapia.
Cáncer de cuello uterino en estadio III
El tratamiento del cáncer de cuello uterino en estadio III puede incluir radioterapia interna y radioterapia externa, combinada con quimioterapia.
Cáncer de cuello uterino en estadio IVAEl tratamiento del cáncer de cuello uterino en estadio IVA puede incluir radioterapia interna y radioterapia externa, combinada con quimioterapia.
Cáncer de cuello uterino en estadio IVB
El tratamiento del cáncer de cuello uterino en estadio IVB puede incluir los siguientes procedimientos:- Radioterapia, como tratamiento paliativo para aliviar los síntomas ocasionados por el cáncer y mejorar la calidad de vida.
- Quimioterapia.
Opciones de tratamiento para el cáncer de cuello uterino recidivante
El tratamiento del cáncer de cuello uterino recidivante puede incluir los siguientes procedimientos:- Exenteración pélvica, seguida de radioterapia combinada con quimioterapia.
- Quimioterapia, como tratamiento paliativo para aliviar los síntomas ocasionados por el cáncer y mejorar la calidad de vida.
Quimioterapia
La quimioterapia es un tratamiento del cáncer que utiliza medicamentos para interrumpir el crecimiento de células cancerosas, mediante su destrucción o evitando su multiplicación. Cuando la quimioterapia se administra oralmente o se inyecta en una vena o músculo, los medicamentos ingresan al torrente sanguíneo y afectan las células cancerosas en todo el cuerpo (quimioterapia sistémica). Cuando la quimioterapia se coloca directamente en la columna vertebral, un órgano o una cavidad corporal como el abdomen, los medicamentos afectan principalmente las células cancerosas en esas áreas (quimioterapia regional). La forma en que se administra la quimioterapia depende del tipo y el estadio del cáncer que está siendo tratado.
Cirugía
Los tumores de cérvix que se diagnostican en fases tempranas, se tratan con la cirugía que suele ser un tratamiento local curativo. Suele ser el primero en llevarse a cabo. Con frecuencia, se añade la radioterapia para completar el tratamiento.
La cirugía oncológica para el cáncer de cérvix es una intervención quirúrgica mayor, por lo que es necesario un ingreso hospitalario durante un tiempo que puede variar de una enferma a otra. Lo más habitual es que oscile de una a dos semanas. Asimismo, es necesario anestesia, que siempre será de tipo general.Radioterapia
En los tumores de cérvix la radioterapia es un tratamiento curativo con los mismos resultados que la cirugía. Su aplicación puede ser externa o interna, aunque generalmente se combinan ambas modalidades.
En la radioterapia externa se emplean equipos generadores de radiación (aceleradores lineales) que en ningún momento contactan con la paciente.
La radioterapia interna consiste en la colocación de materiales radiactivos próximos a la zona tumoral. Se colocan en la cavidad uterina y/o en la vagina, por lo que se denomina radioterapia endocavitaria o intracavitaria. Utiliza una sustancia radiactiva sellada en agujas, semillas, cables o catéteres que se colocan directamente en el cáncer o cerca del mismo. La forma en que se administra la radioterapia depende del tipo y el estadio del cáncer que está siendo tratado.
La radioterapia se puede emplear como tratamiento único o tras la cirugía si existen posibilidades de que reaparezca el tumor en la zona donde estaba situado el mismo. Su objetivo en este caso, es destruir las células tumorales que hayan podido quedar tras la cirugía.
El tratamiento con radioterapia siempre es individualizado, es decir, cada enferma tendrá su tratamiento específico y distinto al de otra paciente.
Según la finalidad con que se emplee, la radioterapia puede ser curativa o paliativa para aliviar síntomas provocados por el cáncer de cérvix tales como dolor, sangrado vaginal, etcPlanificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como la vejiga, el recto o las cabezas femorales. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..
Radioterapia internaEs una técnica de tratamiento que consiste en introducir en el interior del organismo isótopos radiactivos. Se pueden implantar de forma temporal o permanente en la zona a tratar.
Con la radioterapia interna se logra administrar altas dosis de radiación a cortas distancias, de tal forma, que llega muy poca dosis a los tejidos sanos circundantes al implante.
¿Cómo se colocan los implantes?Dependiendo del tipo de implante que se vaya a realizar es necesario permanecer ingresado en el hospital durante 1 o dos días, en otros casos el paciente podrá irse a su casa el mismo día tras recibir el tratamiento. Bajo sedación o anestesia general, se efectuará la colocación de los isótopos radiactivos.
¿Es necesario permanecer aislado?En ocasiones, mientras tenga colocados los implantes es necesario que permanezca en una habitación, preparada especialmente para tal fin.
El paciente estará controlado, en todo momento, a través de un monitor de televisión por el personal sanitario responsable de su cuidado.
¿Cuánto dura el tratamiento?La duración del tratamiento dependerá en gran medida del tipo de isótopo que se haya empleado en el implante y de la cantidad de dosis que se quiera administrar en la zona del tumor, pero generalmente oscila entre minutos y días.
Vacunación contra el cáncer de cérvix
Existen dos vacunas contra la infección de los tipos VPH asociados al cáncer de cérvix. Una de ellas está dirigida contra dos antígenos de VPH más relacionados con el cáncer de cérvix que son el 16 y 18. Se la llama, por ello, bivalente. La otra, llamada tetravalente, va dirigida contra cuatro antígenos del VPH, los tipos 16 y 18, y otros dos más 6 y 11, estos últimos relacionados con las verrugas y condilomas genitales.
Se debe vacunar a las niñas preadolescentes, entre 11 y 14 años. Hay estudios que sugieren que la vacuna también es eficaz en mujeres más mayores, hasta 26 años, así como en niñas desde los 9 años de edad.
La vacunación contra el VPH es más efectiva antes del contacto con el virus, es decir en la etapa prepuberal antes del inicio de las relaciones sexuales.
En líneas generales, la vacuna no tiene ningún efecto secundario. Puede provocar dolor en la zona de la punción, como efecto secundario más frecuente. También se han descrito leves trastornos digestivos y más raramente cansancio. Importante, la vacunación será complementaria pero no debe sustituir las revisiones ginecológicas. Hay que tener en cuenta que la infección no protege contra el 100% de los VPH, ni con otras enfermedades de trasmisión sexual. Se aconseja que se mantengan las revisiones ginecológicas anuales. Probablemente en el fututo, las citologías serán menos frecuentes (cada 3 a 5 años), y se realizará otro tipo de estudio, como por ejemplo estudios virológicos para conocer los tipos de virus que puedan causar las lesiones en el cuello del útero. Cuando todo marche bien, las revisiones también se podrán espaciar más.
- Carcinoma de Nasofaringe (Cáncer)
Cáncer que se forma en los tejidos de la nasofaringe (la parte superior de la garganta detrás de la nariz). La mayoría de los cánceres de la nasofaringe son carcinomas de células escamosas (cáncer que empieza en las células planas de la nasofaringe).
El carcinoma escamoso o epidermoide supone más del 85% de todos los tipos de tumor que pueden surgir en esta localización.
La Organización Mundial de la Salud los divide en tres tipos:
- Tipo I: Carcinoma epidermoide queratinizado.
- Tipo II: Carcinoma epidermoide no queratinizado.
- Tipo III: Carcinoma indiferenciado. En este tipo se incluyen varias variantes como el linfoepitelioma, el anaplásico, el de células claras, etc.
Elección del tratamiento
Una vez que se ha confirmado el diagnóstico de cáncer de nasofaringe y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado para curarla.
El especialista recomendará y explicará las posibilidades de tratamiento más adecuadas en cada caso, para que una vez que el paciente haya recibido la suficiente información pueda, junto con el médico, tomar una decisión.
El tratamiento del cáncer de cavum, como ocurre en la mayoría de los tumores, es multidisciplinar. Distintas especialidades trabajan juntas para combinar terapias y ofrecer al paciente las mayores posibilidades de curación.
En el tratamiento del cáncer de cavum se sigue un protocolo, es decir un conjunto de normas y pautas (plan de tratamiento), establecidas en base a la experiencia científica que se tiene en el tratamiento de este tumor.
Estos protocolos, que se emplean de forma generalizada en todos los hospitales, recogen las indicaciones o limitaciones del tratamiento en función de los siguientes factores:
- Edad del paciente
- Estado general
- Fase o estadio en la que se encuentra la enfermedad (TNM)
- Tipo o histología del tumor
Probablemente, el médico también tendrá en cuenta si además del cáncer de nasofaringe, existen otras enfermedades importantes que puedan dificultar la realización de algún tratamiento específico. Por tanto, el tratamiento propuesto por el especialista no va a ser el mismo en todos los pacientes.Cáncer de la nasofaringe en estadio I
El tratamiento del cáncer de la nasofaringe en estadio I consiste, por lo general, en radioterapia dirigida al tumor y a los ganglios linfáticos del cuello.
Cáncer de la nasofaringe en estadio II
El tratamiento para el cáncer de la nasofaringe en estadio II puede incluir los siguientes procedimientos:- Quimioterapia combinada con radioterapia.
- Radioterapia dirigida al tumor y los ganglios linfáticos del cuello.
Cáncer de la nasofaringe en estadio III
El tratamiento para el cáncer de la nasofaringe en estadio III puede incluir los siguientes procedimientos:- Quimioterapia combinada con radioterapia.
- Radioterapia dirigida al tumor y a los ganglios linfáticos del cuello.
- Radioterapia seguida de cirugía para extirpar los ganglios linfáticos del cuello en donde queda cáncer o en donde reaparece después de la radioterapia.
Cáncer de la nasofaringe en estadio IV
El tratamiento para el cáncer de la nasofaringe en estadio IV puede incluir los siguientes procedimientos:- Quimioterapia combinada con radioterapia.
- Radioterapia dirigida al tumor y a los ganglios linfáticos del cuello.
- Radioterapia seguida de cirugía para extirpar los ganglios linfáticos del cuello en donde queda cáncer o en donde vuelve después de la radioterapia.
- Quimioterapia para el cáncer que hizo metástasis (se diseminó) hasta otras partes del cuerpo.
Opciones de tratamiento para el cáncer de la nasofaringe recidivanteEl tratamiento para el cáncer de la nasofaringe recidivante puede incluir los siguientes procedimientos:
- Radioterapia externa más radioterapia interna.
- Cirugía.
- Quimioterapia
QuimioterapiaLa quimioterapia es un tratamiento para el cáncer para el que se utilizan medicamentos para interrumpir el crecimiento de células cancerosas, ya sea mediante su destrucción o impidiendo su multiplicación. Cuando la quimioterapia se toma por boca o se inyecta en una vena o músculo, los medicamentos ingresan en el torrente sanguíneo y pueden llegar a las células cancerosas de todo el cuerpo (quimioterapia sistémica). Cuando la quimioterapia se coloca directamente en la columna vertebral, un órgano o una cavidad corporal como el abdomen, los medicamentos afectan principalmente a células cancerosas de esas áreas (quimioterapia regional). La forma en que se administra la quimioterapia depende del tipo y el estadio del cáncer que se está tratando.
Cirugía
La cirugía es un procedimiento que se usa para verificar la presencia de cáncer, extirpar el cáncer del cuerpo o reparar una parte del cuerpo. También se llama operación. En ocasiones, se utiliza cirugía para el cáncer de la nasofaringe que no responde a la radioterapia. Si el cáncer se diseminó hasta los ganglios linfáticos, el cirujano puede extirpar los ganglios linfáticos y otros tejidos del cuello.
Radioterapia
El tratamiento con radioterapia siempre es individualizado, es decir, cada enfermo tendrá su tratamiento específico y distinto al de otro paciente, dependiendo de la localización y extensión de la enfermedad.
Dependiendo de la fase en la que se encuentre la enfermedad, la radioterapia puede ser curativa (sobre todo en etapas iniciales) o paliativa con el objetivo de reducir o eliminar los síntomas secundarios a la extensión de la enfermedad en otros órganos.
En este tipo de tumor es necesario que el tratamiento con radiaciones comprenda todo el cuello.
La radioterapia es un tratamiento para el cáncer que utiliza rayos X de alta energía u otros tipos de radiación para destruir células cancerosas o impedir que crezcan. Hay dos tipos de radioterapia. La radioterapia externa utiliza una máquina fuera del cuerpo que envía la radiación hacia el cáncer. La radioterapia interna utiliza una sustancia radiactiva sellada en agujas, semillas, cables o catéteres, que se coloca directamente en el cáncer o cerca del mismo. La forma de administración de la radioterapia depende del tipo y del estadio del cáncer que se está tratando.
La radioterapia externa dirigida a la tiroides o a la hipófisis puede alterar el funcionamiento de la glándula tiroidea. El médico puede examinar la tiroides antes y después del tratamiento para asegurarse de que funciona correctamente. También es importante que un oncólogo revise los dientes, las encías y la boca del paciente, y corrija cualquier problema que haya antes de comenzar con la radioterapia.Planificación del tratamiento con RT:
Una vez que se ha confirmado el diagnóstico de cáncer de nasofaringe y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado para curarla.
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
El especialista recomendará y explicará las posibilidades de tratamiento más adecuadas en cada caso, para que una vez que el paciente haya recibido la suficiente información pueda, junto con el médico, tomar una decisión.
El tratamiento del cáncer de cavum, como ocurre en la mayoría de los tumores, es multidisciplinar. Distintas especialidades trabajan juntas para combinar terapias y ofrecer al paciente las mayores posibilidades de curación.
En el tratamiento del cáncer de cavum se sigue un protocolo, es decir un conjunto de normas y pautas (plan de tratamiento), establecidas en base a la experiencia científica que se tiene en el tratamiento de este tumor.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como los nervios ópticos, la hipófisis o el tronco cerebral, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar. Los más empleados son una máscara de material termoplástico que se adapta al contorno del paciente.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control.- Carciomas Cutáneos (Cáncer)
- Cáncer que se forma en los tejidos de la piel. La mayoría de los cánceres de la piel se forman en las partes del cuerpo expuestas al sol de las personas de edad avanzada o en personas con un sistema inmunitario debilitado.
Los carcinomas cutáneos son los tumores malignos de la piel diferentes a los melanomas.
Con este nombre se engloban dos tipos de tumores:- Carcinomas Epidermoides o escamosos de la piel
- Carcinoma de células basales de la piel
El carcinoma epidermoide de la piel es una proliferación maligna de un tipo de células de la piel, los queratinocitos. Es un tumor con poca capacidad para dar metástasis aunque sí de ser invasivo localmente.Es un tumor muy frecuente, aunque su incidencia es menor que el carcinoma de células basales. Supone el 20-25% de los tumores malignos cutáneos. En los últimos 20 años esta incidencia ha aumentado en casi todos los países, debido a la mayor exposición a la luz solar y a los cambios en el estilo de vestirse.
El carcinoma de células basales procede de la capa más inferior de la epidermis, las células basales. Es particularmente frecuente en la raza blanca, caucasiana. La incidencia está aumentando en un 10% anual.
El factor causal más importante es la luz del sol (ultravioleta), y esto es una constante en todo el planeta. Así la incidencia media en tasa (número de casos por 100.000 habitantes) en Australia es de 1035 casos en hombres y 472 en mujeres, mientras que en Finlandia es solo de 6 y 4, respectivamente. Indudablemente estas cifras varían en función de la raza y del color de la piel. Las razas caucásicas, de piel blanca, son las que más predisposición tienen a este tipo de tumor.
La incidencia aumenta mucho con la edad, resultando muy raro antes de los 45 años.
La luz ultravioleta es absorbida por el DNA de las células de la piel causando daños en el mismo. Si este daño no es reparado por los genes que realizan este trabajo, los trastornos genéticos en la célula se acumulan produciendo su transformación maligna.La presencia de mutaciones en estos genes encargados de la reparación del DNA favorece el desarrollo de estos tumores.
En el carcinoma epidermoide de piel es muy importante el acúmulo de horas de exposición al sol a lo largo de la vida, más que la intensidad de la exposición a la luz solar, que en cambio es un factor más importante para el desarrollo del melanoma y del carcinoma de células basales.
La exposición a radiaciones ionizantes también es un factor de riesgo para los tumores cutáneos no-melanoma, sobre todo el carcinoma de células basales.
Las enfermedades que causan inmunosupresión, como el SIDA, uso crónico de esteroides y tratamiento inmunosupresor por transplantes de órganos, también aumentan la incidencia de los carcinomas cutáneos no-melanoma.
La enfermedades inflamatorias crónicas de la piel, o lesiones inflamatorias de larga duración, como escaras, quemaduras, úlceras etc.. también son situaciones de mayor riesgo para desarrollar un carcinoma cutáneo epidermoide. Enfermedades de la piel que se consideran precancerosas para estos tumores son: xeroderma pigmentosum, epidermodisplasia verruciforme y albinismo.La infección por el papiloma virus en estos pacientes de mayor riesgo, puede aumentar todavía más la probabilidad de tener un carcinoma epidermoide de la piel.
Para el carcinoma de células basales existe una enfermedasd genética predisponerte, llamada síndrome del nevus de células basales, que afortunadamente es rara.Eleccion de TratamientoEl carcinoma escamoso o epidermoide de la piel, así como el de células basales es un tumor localizado a la epidermis en la gran mayoría de los casos. El tratamiento local es, pues, el pilar del tratamiento.
Carcinoma de células basales
El tratamiento del carcinoma de células basales puede incluir los siguientes procedimientos:- Cirugía micrográfica de Mohs.
- Escisión simple.
- Electrodesecación y legrado.
- Criocirugía.
- Radioterapia.
- Cirugía láser.
- Quimioterapia tópica con fluorouracilo.
- Terapia fotodinámica.
Los exámenes de seguimiento de la piel son importantes para las personas con carcinoma de células basales porque tienen más probabilidades de contraer un tumor nuevo o recidivante dentro de los cinco años del primero. Después del tratamiento, el paciente debe someterse a exámenes de la piel cada seis meses durante cinco años y una vez al año a continuación.
Carcinoma de células escamosas
El tratamiento del carcinoma de células escamosas puede incluir los siguientes procedimientos:- Cirugía micrográfica de Mohs.
- Escisión simple.
- Electrodesecación y legrado.
- Criocirugía.
- Radioterapia.
- Quimioterapia tópica con fluorouracilo.
- Cirugía láser.
Los exámenes de seguimiento de la piel son importantes para las personas con carcinoma de células escamosas porque estos carcinomas se pueden diseminar. Los pacientes se deben someter a exámenes de la piel cada tres meses durante varios años después del tratamiento y cada seis meses en adelante.
CrioterapiaDestruye a las células tumorales por congelación. Es una técnica útil en lesiones pequeñas, bien definidas y de bajo riesgo de recidiva. Se utiliza la aplicación de nitrógeno líquido sobre la lesión tumoral y un perímetro de tejido sano superior a 3 mm.
Esta técnica solamente la pueden realizar médicos experimentados y con gran conocimiento de esta enfermedad. Es imposible el estudio histológico de la lesión una vez tratada.
Electrocirugía
También se le llama curetaje o electrodisección.
También es una técnica a aplicar solamente en lesiones pequeñas, bien delimitadas y de bajo riesgo de recaída. Tampoco permite el estudio histológico de la lesión.Tratamiento tópico
Un agente quimioterapéutico, el 5-Fluoruracilo, puede utilizarse de forma tópica y es muy útil para las queratosis actínicas, los carcinomas in situ e incluso en los carcinomas superficiales.
Es de especial valor cuando no son aplicables otras técnicas. Tiene como limitación el que el producto no se extienda a una concentración adecuada sobre la zona a tratar, contribuyendo entonces a que aparezcan recidivas. Se aplica en forma de crema, dos veces al día y durante 4 a 8 semanas. Produce una reacción inflamatoria que puede ser dolorosa. No se debe de aplicar nunca, por ello, cerca de los ojos, labios o fosas nasales.
Otro tratamiento tópico es la Terapia Fotodinámica que se basa en unas sustancias llamadas porfirinas, que tienen capacidad fotosensibilizadora, produciendo daño celular ante la exposición a la luz y en presencia de oxígeno. La aplicación tópica o inyectable de estas sustancias puede permitir la destrucción selectiva de los carcinomas cutáneos superficiales.Cirugía
La extirpación quirúrgica es el tratamiento más ampliamente utilizado. Es una técnica bien tolerada, extremadamente eficaz y que permite estudiar por completo la extensión de la lesión tumoral y asegurar la eliminación de la misma mediante el estudio de los márgenes quirúrgicos.
La extirpación puede realizarse habitualmente con anestesia local y sin necesidad de ingreso hospitalario.
En los tumores superficiales la curación se consigue en el 92% de los casos. Cuando el tumor tiene una invasión en profundidad o afectación ganglionar regional la extirpación quirúrgica consigue la curación en el 72% de los casosRadioterapia
Es una buena elección para tratar tumores pequeños, bien delimitados y especialmente en personas mayores o en las que no se considera indicado un tratamiento quirúrgico.
Es una técnica de tratamiento contraindicada en los tumores de células basales y en el carcinoma verrucoso.
La radioterapia también se utiliza cuando el tumor primario no se puede resecar por completo o cuando los ganglios regionales están afectadosPlanificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como glándulas salivales o cualquier órgano de riesgo cercano al área de irradiar. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar. Los más empleados son una máscara de material termoplástico que se adapta al contorno del paciente.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control. - Cerebro (Cáncer)
Cuando las células que constituyen dicho tumor no poseen la capacidad de invadir y destruir otros órganos, hablamos de tumores benignos. Pero cuando estas células además de crecer sin control sufren nuevas alteraciones y adquieren la facultad de invadir tejidos y órganos de alrededor (infiltración), y de trasladarse y proliferar en otras partes del organismo (metástasis), se denomina tumor maligno, que es a lo que llamamos cáncer.
La malignidad de un tumor viene determinada por la agresividad de sus células, que le confiere una mayor o menor capacidad de invasión.
Cuando estas alteraciones aparecen en cualquiera de las estructuras que forman el sistema nerviosos central hablamos de tumores del sistema nerviosos central, que dependiendo de su localización serán tumores cerebrales, cerebelosos, del tronco cerebral…
Asimismo estos tumores se clasifican en función de la célula de la que proceden, así los que se originan en los astrocitos se denominan astrocitomas, en los oligodendrocitos oligodendrogliomas, etc.
Una característica típica de los tumores cerebrales, a diferencia de tumores malignos de otras localizaciones, es que con poca frecuencia se diseminan fuera del SNC.
Tipos de tumores del SNC
Los tumores del SNC pueden ser primarios o secundarios
Los tumores primarios son aquellos que se originan en las distintas células cerebrales. Estos pueden ser malignos o benignos dependiendo de las características de las células que lo forman.
Los tumores secundarios son aquellos que se desarrollan en el cerebro como consecuencia de la diseminación de células de un tumor maligno que puede estar localizado en cualquier órgano del cuerpo.
La localización dónde inicialmente se origina un cáncer se denomina tumor primario. Cuando las células malignas se diseminan a otros órganos, se implantan y crecen en ellos dando lugar a tumores secundarios o metástasis. Las células que forman estas metástasis son similares a las del tumor primario.
A los tumores secundarios cerebrales también se les denomina metástasis cerebrales.
Los cánceres que con más frecuencia producen metástasis cerebrales son los de pulmón, mama, colon, riñón, vejiga y melanoma.
Tipos de tumor primario
Los tumores primarios del SNC reciben el nombre en función de la célula en la que se originan. Los más frecuentes son los siguientes:
Gliomas: Se originan a partir de las células de soporte del tejido nervioso, denominadas células gliales. Más de la mitad de los tumores del SNC son gliomas.
Clasificación de los gliomas
Se clasifican en función de la velocidad de división y del aspecto que poseen las células cuando se observan al microscopio.
Los gliomas se dividen en 4 grados:- Grado 1 y 2: también denominados gliomas de bajo grado. Están constituidos por células que se dividen lentamente y suelen ser poco agresivos.
- Grado 3 y 4: o gliomas de alto grado. En ambos casos sus células se dividen más rápidamente y son de mayor malignidad que los gliomas grado 1 y 2.
El tratamiento y el pronóstico dependen fundamentalmente del grado del tumor.
Tipos de gliomas
Astrocitomas: Los astrocitomas grado 3 también se denominan astrocitomas anaplásicos y los tumores grado 4 reciben el nombre de glioblastomas multiformes (supone el 30% del total de tumores cerebrales en el adulto). Ambos, son los tumores de células gliales más frecuentes del adulto y proceden de los astrocitos.
Oligodendrogliomas: proceden de los oligodendrocitos, que son las células encargadas de la producción del tejido que recubre los distintos nervios (la mielina, que se encarga de facilitar la conducción de los impulsos nerviosos entre las fibras nerviosas). Son de crecimiento más lento que los astrocitomas.
Glioma Mixto: Está constituido por varios tipos de células, siendo los más frecuentes los oligo-astrocitomas
Ependimomas: son tumores poco frecuentes, representan el 9% de todos los tumores cerebrales. Es más frecuente en la infancia y adolescencia. Proceden de las células que recubren los ventrículos y el canal medular. A través del líquido cefalorraquídeo pueden diseminarse por todo el sistema nervioso central.
Se dividen en ependimomas de bajo grado o benignos, que son los más frecuentes o ependimomas de alto grado o anaplásicos.
Méduloblastoma: Es el segundo tumor cerebral más frecuente en el niño, aunque un 30% aparece en adultos. Su localización habitual es en el cerebelo.
El méduloblastoma es un tumor invasivo y de rápido crecimiento y con frecuencia se disemina a otras partes del sistema nervioso central.
Meningioma o tumor neuroectodérmico primitivo: Es un tumor, generalmente benigno que se desarrolla a partir de las meninges (tejido que recubre el sistema nerviosos central). Representa el 20% de todos tumores cerebrales primarios y, se suelen localizar con más frecuencia en los hemisferios cerebrales, aunque también pueden aparecer en la médula espinal.
Los síntomas de este tumor son secundarios a la compresión de tejido cerebral sano, más que a una invasión del mismo.
Cráneofaringioma: Es un tumor benigno congénito por lo que aparece fundamentalmente en la infancia y adolescencia.Crecen en una zona del cerebro denominada la silla turca, donde se sitúa la glándula pituitaria y muy próxima a los nervios ópticos. Los síntomas suelen ser debidos a aumento de la presión intracraneal.
Cordomas: Supone el 2% del total de tumores primarios del sistema nervioso central, siendo más frecuente en adultos jóvenes (entre la 2ª y la 4ª década). Se localizan en la base del cráneo y en la porción final de la médula espinal. Este tumor es generalmente benigno, aunque suele invadir hueso por contigüidad.Linfoma primario del sistema nervioso central: Su localización más frecuente es en los hemisferios del cerebro. Son tumores del sistema linfático, que forma parte del sistema inmunológico del organismo, por lo que suelen aparecer en pacientes inmunodeprimidos (pacientes sometidos a trasplante de órganos o con SIDA).
Adenomas de la glándula pituitaria: La glándula pituitaria produce una serie de hormonas que se encargan de controlar la producción hormonal de las otras glándulas del cuerpo.
Los adenomas pituitarios son tumores benignos, de crecimiento lento y suponen el 8% de todos los tumores primarios del SNC.Estos tumores se clasifican en tumores secretores y no secretores en función de su capacidad para segregar o no segregar una determinada hormona.
Elección del tratamiento
El especialista recomendará y explicará las posibilidades de tratamiento más adecuadas en cada caso, para que una vez que el paciente haya recibido la suficiente información pueda, junto con el médico, tomar una decisión..
El tratamiento de los tumores del SNC, como ocurre en la mayoría de los cánceres, es multidisciplinar. Distintas especialidades trabajan juntas para combinar terapias y ofrecer al paciente las mayores posibilidades de curación.
En el tratamiento de estos tumores se sigue un protocolo, es decir un conjunto de normas y pautas (plan de tratamiento), establecidas en base a la experiencia científica que se tiene en el tratamiento de este tumor.
Estos protocolos, que se emplean de forma generalizada en todos los hospitales, recogen las indicaciones o limitaciones del tratamiento en función de los siguientes factores:- Edad del paciente
- Estado general
- Tipo de tumor
- Localización del tumor
Probablemente, el médico también tendrá en cuenta si además del tumor de SNC existen otras enfermedades importantes que puedan dificultar la realización de algún tratamiento específico.
Por tanto, el tratamiento propuesto por el especialista no va a ser el mismo en todos los pacientes.
Los tratamientos más frecuentemente empleados son la cirugía, la radioterapia y en algunos casos la quimioterapia.Cirugía
La cirugía es el tratamiento de elección para los tumores del SNC accesibles, es decir que pueden ser extirpados sin causar un daño neurológico importante.
El objetivo fundamental de la cirugía es la extirpación de todo el tejido tumoral visible, sin embargo, una extirpación parcial del mismo (cirugía reductora) puede ser beneficioso para el paciente, ya que disminuyen los síntomas provocados por el aumento de la presión intracraneal, mejora la calidad de vida del paciente y reduce el volumen tumoral para tratamientos posteriores.
La cirugía también es útil para establecer el diagnóstico, mediante la obtención de una muestra del tejido tumoral (biopsia) y su posterior análisis al microscopio. La realización de una biopsia (es decir sin extirpar el tumor) sólo se realiza cuando el tumor es inoperable, ya que siempre que sea posible se debe llevar a cabo una extirpación del mismo.
La mayoría de los tumores benignos del SNC se tratan con cirugía exclusiva, mientras que los tumores malignos necesitan tratamiento adicional generalmente con radioterapia.
Si un tumor no ha podido ser extirpado en su totalidad, o existe sospecha de que hayan podido quedar células tumorales en la zona de la intervención, es necesario administrar radioterapia complementaria a la cirugía.
Cuando un tumor es inoperable, el tratamiento principal se realiza con radioterapia acompañada o no de quimioterapia.Radioterapia
En los tumores cerebrales, la radioterapia está indicada tras la cirugía con el fin de eliminar las células o el resto de tumor que haya podido quedar tras la intervención; o cuando un tumor no se puede operar, bien por su inaccesibilidad o bien porque es inoperable, como ocurre con las metástasis cerebrales.
Según la finalidad con que se emplee, la radioterapia puede ser curativa o paliativa para aliviar síntomas provocados por el tumor.
Radioterapia Esterotáxica Fraccionada
Es una modalidad de radioterapia que se administra con aceleradores lineales adaptados para este tratamiento y consiste en la administración de una alta dosis de radiación en la zona del tumor (previamente localizada mediante un TC o una resonancia Magnética) a lo largo de varias sesiones.
Para tratar esta zona se emplean múltiples campos o arcos (el brazo del acelerador lineal se mueve durante el tratamiento), con la finalidad de proporcionar altas dosis de radiación a la zona del tumor evitando la irradiación innecesaria en los tejidos sanos circundantes. Para ello es necesario sistemas de inmovilización del paciente muy precisos (guía).
Es una técnica no invasiva, no dolorosa y no requiere hospitalización del paciente.Radiocirugía
La radiocirugía consiste en la aplicación de una dosis única de radiación de alta energía al tumor.
Aunque se denomina radiocirugía no implica ninguna intervención quirúrgica, es decir, no se realiza ninguna incisión y se puede administrar en régimen ambulatorio. Con esta técnica se evitan las complicaciones, la hospitalización y el tiempo de recuperación asociado con la cirugía craneal convencional.
La radiocirugía permite irradiar un tumor cerebral con gran precisión. Este tratamiento es posible gracias al uso de un marco estereotáxico o guía esterotáxica, mínimamente invasivo que mantiene al paciente perfectamente posicionado. El marco estereotáxico es un anillo metálico que forma un círculo alrededor de la cabeza y se fija a los huesos del cráneo.
Esta técnica minimiza la radiación del tejido cerebral sano, y protege los órganos vecinos.
El procedimiento no es doloroso, y ayuda a evitar largos períodos de hospitalización o rehabilitación y manteniéndose el paciente despierto durante todo el tratamiento. Se puede recibir el tratamiento por la mañana y regresar a la rutina habitual por la tarde.- Colon (Cáncer)
Cáncer que se presenta en los tejidos del colon (la parte más larga del intestino grueso). La mayoría de los cánceres de colon son adenocarcinomas (cánceres que empiezan en las células que producen y liberan el moco y otros líquidos).
La mayoría de los cánceres colorrectales aparecen sobre un pólipo existente en la mucosa del colon o recto, que por diversas circunstancias evoluciona a tumor maligno. La gran mayoría de los tumores malignos colorrectales se desarrollan sobre lesiones ya existentes en la mucosa, como pueden ser pólipos o enfermedades inflamatorias. El cáncer que aparece en una mucosa sana es excepcional.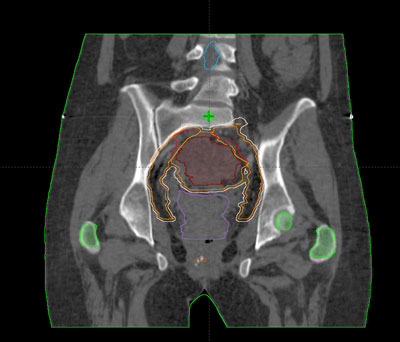
El tipo de cáncer colorrectal más frecuente es el adenocarcinoma. Aparece en el 90-95% de los casos y se produce en la mucosa que recubre el interior del colon y recto.
Existen otros tipos de tumores que pueden localizarse en colon y recto, aunque con una escasa frecuencia de aparición, como son:- Sarcomas: tumores originados en la capa muscular del tubo digestivo.
- Linfomas: cáncer de las células de la defensa del estómago e intestino.
- Tumores carcinoides: de las células productoras de hormonas del aparato digestivo.
- Melanomas
El hecho de que el tumor sea menos frecuente no quiere decir que su pronóstico sea peor, sino diferente al tipo de tumor de mayor incidencia en colon y recto.
Para poder determinar el tratamiento más adecuado para el cáncer colorrectal, es importante clasificar el tumor, es decir, determinar en qué fase se encuentra.
Existen dos sistemas de clasificación que se utilizan con igual frecuencia en el cáncer de colon y recto:- Clasificación TNM
- Clasificación de Astler y Coller
1.Clasificación TNM: Estas siglas hacen referencia a tres aspectos del cáncer: la T se refiere al tamaño del mismo, la N a la afectación de los ganglios linfáticos y la M a la afectación o no de otros órganos. En función de estos aspectos, el cáncer colorrectal se agrupa en las siguientes etapas o estadios:
Estadio 0 o carcinoma in situ: es la fase más temprana del cáncer de colon o recto. Las células tumorales se encuentran situadas en la parte más superficial de la mucosa y en ningún caso la traspasa. No afecta a ganglios linfáticos.Estadio I: el tumor afecta a la pared del colon o recto sin traspasar la capa muscular. No existe afectación de ganglios linfáticos.
Estadio II: el tumor ha infiltrado todas las capas de la pared del colon o recto. Puede invadir los órganos de alrededor. No se aprecia afectación ganglionar.
Estadio III: el cáncer ha invadido a los órganos más próximos y afecta a los ganglios linfáticos.
Estadio IV: el cáncer se ha diseminado afectando a órganos alejados del colon o recto como hígado, pulmón o huesos.
2.Clasificación de Astler y Coller: en esta clasificación se utilizan las letras que van desde la A hasta la D.
Estadio A: lesión limitada a la mucosa, sin afectación ganglionar.
Estadio B1: el tumor afecta a parte de la pared del colon o recto, sin atravesarla ni afectar ganglios.
Estadio B2: afecta a toda la pared sin invasión ganglionar.
Estadio C: la enfermedad puede afectar a parte o a toda la pared, con afectación ganglionar.
Estadio D: existe afectación de otros órganos alejados.
Elección del tratamiento
Una vez que se ha confirmado el diagnóstico de cáncer colorrectal y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado para curarla. El especialista le recomendará y explicará las posibilidades de tratamiento más adecuadas en su caso, para que una vez que haya recibido la suficiente información pueda, junto con su médico tomar una decisión.
El tratamiento del cáncer colorrectal, como ocurre en la mayoría de los tumores, es un tratamiento multidisciplinar. Distintas especialidades trabajan juntas para combinar terapias y ofrecer al paciente las mayores posibilidades de curación.
En el tratamiento del cáncer colorrectal se sigue un protocolo, es decir, un conjunto de normas y pautas (plan de tratamiento) que se establecen, basándose en la experiencia científica, para el tratamiento de dicho tumor.
Estos protocolos, que se emplean de forma generalizada en todos los hospitales, recogen las indicaciones o limitaciones de tratamiento en función de una serie de factores:- Estado general del paciente.
- Localización del tumor.
- Fase en la que se encuentra la enfermedad: infiltración en la pared del colon o recto, afectación ganglionar, afectación de órganos próximos y diseminación de la enfermedad.
El médico también tendrá en cuenta, si además del cáncer colorrectal, existen otras enfermedades importantes que puedan dificultar la realización de algún tratamiento específico. Por tanto el tratamiento propuesto por el especialista no va a ser el mismo en todos los pacientes.
Los tratamientos más frecuentemente empleados en el cáncer de colon son la cirugía, la radioterapia y la quimioterapia.
Estadio 0 (carcinoma in situ)
El tratamiento del estadio 0 (carcinoma in situ) puede incluir los siguientes tipos de cirugía:
- Escisión local o polipectomía simple.
- Resección /anastomosis. Esto se lleva a cabo cuando el tumor es demasiado grande para extirparse por escisión local.
Cáncer del colon en estadio I
El tratamiento del cáncer de colon en estadio I generalmente comprende resección /anastomosis.
Cáncer del colon en estadio II
El tratamiento del cáncer de colon en estadio II generalmente comprende los siguientes procedimientos:- Resección /anastomosis.
Cáncer del colon en estadio III
El tratamiento del cáncer de colon en estadio III puede incluir los siguientes procedimientos:- Resección /anastomosis con quimioterapia.
Cáncer del colon en estadio IV y recidivanteEl tratamiento del cáncer de colon en estadio IV y recidivante puede incluir los siguientes procedimientos:
- Resección /anastomosis (cirugía para extirpar el cáncer o derivar el tumor y unir los extremos cortados del colon).
- Cirugía para extirpar partes de otros órganos como el hígado los pulmones y los ovarios a los que el cáncer se puede haber diseminado o vuelto.
- Se puede ofrecer radioterapia o quimioterapia a algunos pacientes como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
El tratamiento para el cáncer recurrente del colon puede incluir la escisión local.
Los tratamientos especiales para el cáncer que se ha diseminado o regresado al hígado pueden incluir los siguientes procedimientos: - Quimioterapia seguida de resección.
- Ablación por radiofrecuencia o criocirugía.
A los pacientes en los que el cáncer del colon se disemina o vuelve después del tratamiento inicial con quimioterapia, se les puede ofrecer quimioterapia adicional con un medicamento diferente o una combinación de medicamentos.
Quimioterapia
La quimioterapia es un tratamiento para el cáncer en el que se usan medicamentos para interrumpir el crecimiento de células cancerosas, ya sea mediante su destrucción o impidiendo su multiplicación. Cuando la quimioterapia se toma por boca o se inyecta en una vena o músculo, los medicamentos ingresan en la corriente sanguínea y pueden llegar a las células cancerosas de todo el cuerpo (quimioterapia sistémica). Cuando la quimioterapia se coloca directamente en la columna vertebral, un órgano o una cavidad corporal como el abdomen, los medicamentos afectan principalmente las células cancerosas de esas áreas (quimioterapia regional).
La quimioembolización de la arteria hepática se puede utilizar como tratamiento para el cáncer que se ha diseminado hasta el hígado. Esto implica la obstrucción de la arteria hepática (la arteria principal que suministra sangre al hígado) y la inyección de medicamentos anticancerosos entre el bloqueo y el hígado. Las arterias del hígado se encargan entonces de repartir los medicamentos a través del hígado. Solo una pequeña cantidad del medicamento se extiende a otras partes del cuerpo. El bloqueo puede ser temporal o permanente, dependiendo de lo que se utiliza para bloquear la arteria. El hígado continúa recibiendo un poco de sangre de la vena porta hepática, que lleva la sangre desde el estómago y el intestino.
La forma en que se administra la quimioterapia depender del tipo y el estadio del cáncer que se está tratando.
Cirugía
La cirugía suele ser el tratamiento más importante y el primero en llevarse a cabo en la mayoría de los tumores de colon.
El tipo de cirugía que se puede aplicar en el cáncer colorrectal, varía en función de su localización y de la extensión a ganglios y/u órganos vecinos.
La cirugía a nivel del colon y recto es una intervención quirúrgica mayor, por lo que es necesario el ingreso hospitalario durante un tiempo que puede variar de un enfermo a otro. Lo más habitual es que oscile entre una y dos semanas. Asimismo, es necesaria anestesia, que siempre será de tipo general.
La cirugía suele ser el principal tratamiento local para el cáncer de colon. La técnica consiste en la extirpación del segmento del colon en el que se asienta el tumor, así como un tramo de tejido normal a cada lado de la lesión y los ganglios linfáticos correspondientes. Posteriormente, se unen los extremos del colon para restablecer la continuidad del tubo digestivo y mantener su función intacta.
Generalmente, este tipo de intervención no suele provocar efectos secundarios severos y el paciente puede salir del hospital entre 5 y 7 días tras la cirugía, aunque la hospitalización y recuperación dependerán de las condiciones de salud específicas de cada enfermo.
En el caso de que sea necesario hacer una colostomía, es aconsejable que hable con el personal de enfermería encargado de realizar el cuidado de la ostomía, de tal forma que le puedan resolver las dudas.
En los casos en que exista una afectación hepática pequeña suele extirparse la zona de la metástasis.
En ocasiones, cuando la invasión local por el tumor es importante y no es posible extirparlo en su totalidad, se puede llevar a cabo una intervención con finalidad paliativa. La intervención consiste en conectar la zona previa y la posterior del tumor empleando un asa intestinal, de tal forma que las heces no tengan que pasar la zona de colon afectada por la lesión.La ostomía
La ostomía es la intervención quirúrgica que permite comunicar una víscera con el exterior. Cuando se comunica el colon con la pared abdominal se denomina colostomía. La abertura externa se llama estoma.
La colostomía puede ser temporal o permanente, siendo esta última la que con mayor frecuencia se lleva a cabo en el cáncer colorrectal. En el caso de la colostomía temporal se restablece el tránsito intestinal uniendo los extremos seccionados del colon pasado un tiempo.
La colostomía permanente se produce como consecuencia de la extirpación del ano por lo que no es posible realizar reconstrucción, quedando la colostomía de forma definitiva permitiendo la salida de heces al exterior.
La función del esfínter anal es posibilitar el control de la evacuación de las heces de manera voluntaria. Cuando es necesario extirpar el recto por un cáncer, el estoma se sitúa en la parte baja del lado izquierdo y las heces que se expulsan, tendrán una consistencia sólida y se recogerán en un sistema colector (bolsa).
Radioterapia
La radioterapia tiene un papel importante en el tratamiento del cáncer de recto, mientras que en el de colon no se emplea de forma rutinaria. Esto es debido a que la evolución de estos tumores es diferente. Mientras que el cáncer de recto tiende a reaparecer en la zona de la intervención, el cáncer de colon lo hace en otros órganos como por ejemplo en el hígado.
En el cáncer de recto se utiliza tanto la radioterapia externa como la interna, aunque la más frecuente es la externa. En cualquier caso es el oncólogo radioterapeuta quien prescribe y planifica el tratamiento con radioterapia.
La finalidad de la radioterapia varía en función del momento en que se administre:- Previa a la cirugía: el objetivo es reducir el tamaño del tumor permitiendo realizar una cirugía conservadora en determinados casos y disminuye la posibilidad de que se diseminen células durante la cirugía.
- Posterior a la cirugía: permite destruir las células tumorales que hayan podido quedar tras la intervención.
El tratamiento con radioterapia siempre es individualizado, es decir, cada enfermo tendrá su tratamiento específico y distinto al de otro paciente.Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como los riñones, la vejiga, el recto, las cabezas femorales. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control.
-
E
- Esófago (Cáncer)
Cáncer que se forma en los tejidos que revisten el esófago (el tubo muscular a través del cual pasan los alimentos desde la garganta hasta el estómago). Dos tipos de cáncer de esófago son el carcinoma de células escamosas (cáncer que comienza en las células planas que recubren el esófago) y el adenocarcinoma (cáncer que comienza en las células que producen y liberan moco y otros líquidos).
La mayoría de los cánceres de esófago ocurren en su tercio inferior y en la zona de unión con el estómago (unión gastro-esofágica). En esta localización la variedad histológica es la de Adenocarcinoma. Menos frecuentemente aparece en las porciones altas del conducto siendo la variedad histológica el carcinoma epidermoide o escamoso.
Las formas más comunes de cáncer de esófago reciben nombres que dependen del tipo de célula del que se derivan:
La mucosa del esófago está formada por células planas llamadas escamosas, por lo que el tumor derivado de ellas se denominará carcinoma escamoso o epidermoide (estas células recuerdan a las de la piel o epidermis). Es el tipo de cáncer más frecuente en esta localización, especialmente en el esófago proximal (tercio superior) y medio.
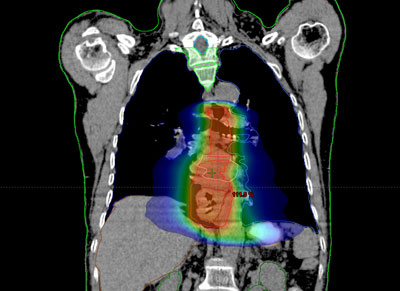
En el esófago de Barrett la mucosa se cambia por otra de tipo glandular o adenoide por lo que el tumor derivado de dichas células se denomina adenocarcinoma. Ocurre casi siempre en el tercio inferior del esófago, y siempre es necesario que exista previamente esa alteración de la mucosa.
Aunque más raramente, la pared esofágica puede ser asiento de tumores no epiteliales (carcinomas).
Uno de los tumores más frecuentes de este grupo es el que procede del estroma (GIST), que tiene un comportamiento variable (potencialmente maligno). Este tipo de tumores no entran en la definición de cáncer de esófago. Su pronóstico y tratamiento son completamente diferentes
Para poder determinar el tratamiento más adecuado para el cáncer de esófago, es importante clasificar el tumor, es decir, determinar en qué fase se encuentra.El sistema que con mayor frecuencia se emplea para su clasificación es el TNM. Estas siglas hacen referencia a tres aspectos del cáncer:
La T se refiere al nivel de extensión o penetración del tumor primario en las paredes del esófago:
- Tis: es el tumor “in situ”, confinado a la mucosa.
- T1: tumor que invade la llamada lámina propia (T1a) o la submucosa (T1b).
- T2: Tumor que invade la muscularis propia
- T3: tumor que invade la adventicia
- T4: Tumor que invade estructuras adyacentes.
La N se refiere a la presencia o no de afectación de los ganglios linfáticos regionales o más próximos a la zona donde se origina el tumor.
- N0 significa ausencia de afectación ganglionar
- N1 significa la presencia de afectación tumoral en algún ganglio linfático regional
La M se refiere a la presencia confirmada de metástasis a distancia:
- M0 es ausencia de metástasis
- M1 es presencia de metástasis a distancia.
Elección del tratamiento
Una vez que se ha confirmado el diagnóstico de cáncer de esófago y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado para curar la enfermedad. El especialista le recomendará y explicará las posibilidades de tratamiento más adecuadas en su caso, para que una vez que haya recibido la suficiente información pueda, junto con su médico tomar una decisión.
El tratamiento del cáncer de esófago, como ocurre en la mayoría de los tumores, es un tratamiento multidisciplinar. Distintas especialidades trabajan juntas para combinar terapias y ofrecer al paciente las mayores posibilidades de curación.En el tratamiento del cáncer de esófago se sigue un protocolo, es decir, un conjunto de normas y pautas (plan de tratamiento) que se establecen, basándose en la experiencia científica, para el tratamiento de dicho tumor.
Estos protocolos, que se emplean de forma generalizada en todos los hospitales, recogen las indicaciones o limitaciones de tratamiento en función de una serie de factores:
- Fase en la que se encuentra la enfermedad (TNM).
- La localización del cáncer: el tratamiento puede variar dependiendo de si la enfermedad está localizada en el tercio superior, medio o inferior.
El médico también tendrá en cuenta, si además del cáncer de esófago, existen otras enfermedades importantes (enfermedades concomitantes, como cardiopatía isquémica, hipertensión, arteriosclerosis, edad etc..) que puedan dificultar la realización de algún tratamiento específico.
Por tanto el tratamiento propuesto por el especialista no va a ser el mismo en todos los pacientes, sino que se tiene que adaptar a las condiciones particulares de cada persona con esta enfermedad.
Los tratamientos más frecuentemente empleados en el cáncer de esófago son, fundamentalmente, la cirugía, la radioterapia y la quimioterapia.Estadio 0 (carcinoma in situ)
El tratamiento habitual del estadio 0 es la cirugía.
Cáncer del esófago en estadio IEl tratamiento del cáncer de esófago en estadio I puede incluir los siguientes procedimientos:
- Cirugía.
Cáncer del esófago en estadio IIEl tratamiento del cáncer de esófago en estadio II puede incluir los siguientes procedimientos:
- Cirugía.
- Quimiorradiación (tratamiento que combina quimioterapia con radioterapia).
Cáncer del esófago en estadio IIIEl tratamiento del cáncer de esófago en estadio III puede incluir los siguientes procedimientos:
- Cirugía.
- Quimiorradiación (tratamiento que combina quimioterapia con radioterapia).
Cáncer del esófago en estadio IVEl tratamiento del cáncer de esófago en estadio IV puede incluir los siguientes procedimientos:
- Colocación de una cánula esofágica como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
- Radioterapia externa o radioterapia interna, como tratamiento paliativa para aliviar los síntomas y mejorar la calidad de vida.
- Cirugía láser o electrocoagulación, como tratamiento paliativo para aliviar los síntomas y mejorar la calidad de vida.
- Quimioterapia.
Opciones de tratamiento para el cáncer de esófago recidivante
El tratamiento del cáncer de esófago recidivante puede incluir los siguientes procedimientos:
- Utilización de cualquier tratamiento estándar, como tratamiento paliativo para aliviar los síntomas y mejorar la calidad de vida.
Cirugía
El tipo de cirugía que se puede aplicar en el cáncer de esófago, varía en función del tamaño, de la localización y de la extensión de la enfermedad a ganglios y/o órganos vecinos.
La técnica más frecuente es la extirpación de parte o de la totalidad del esófago. Esta intervención se denomina esofagectomía.
El cirujano extirpa la zona del esófago en la que se encuentra el tumor con una porción de esófago sano a ambos lados. Posteriormente, se conectan la parte sana del esófago con el estómago para que el paciente pueda tragar. En ocasiones, si la zona que ha extirpado el cirujano es muy amplia y no se puede unir los extremos del esófago y el estómago, se utiliza una zona del colon como prótesis para posibilitar la unión entre ambos.Quimioterapia
En el cáncer de esófago cuando el tumor no se puede operar, la quimioterapia se aplica generalmente asociada a la radioterapia para potenciar el efecto de esta última sobre el tumor y lograr así su desaparición. Al administrar ambos tratamientos conjuntamente, es frecuente que aumenten los efectos secundarios.
En ocasiones puede administrarse antes de la cirugía para disminuir el tamaño del tumor y facilitar así su extracción ( se le llama tratamiento neoadyuvante).
Si el tumor está diseminado, la quimioterapia se utiliza como tratamiento único y su objetivo, fundamental, es disminuir los síntomas derivados del tumor y mejorar la calidad de vida del paciente.Radioterapia Esófago
La radioterapia es el empleo de radiaciones ionizantes para el tratamiento, local o locorregional, de determinados tumores que emplea rayos X con altas dosis de irradiación.
Su objetivo es destruir las células tumorales causando el menor daño posible a los tejidos sanos que rodean dicho tumor.
En la mayoría de los tumores de esófago, la radioterapia que se aplica es externa. Para ello se emplean máquinas de gran tamaño (aceleradores lineales) que, en ningún momento contactan con el enfermo. En ocasiones, la radioterapia puede ser interna. En estos casos se coloca un material radiactivo (isótopo) en forma de dispositivo metálico en contacto con el tumor.
La radioterapia se puede emplear como tratamiento único o en combinación. Se puede administrar antes de la intervención para disminuir su tamaño y facilitar la cirugía (tratamiento neoadyuvante), o después de la misma, para "limpiar" la zona de la cirugía de las posibles células tumorales que hayan podido quedar (tratamiento adyuvante).Asimismo, se puede administrar con la quimioterapia para potenciar sus efectos (quimioirradiación).
El tratamiento con radioterapia siempre es individualizado, es decir, cada enfermo tendrá su tratamiento específico y distinto al de otro paciente.
Según la finalidad con que se emplee, la radioterapia puede ser curativa o paliativa para aliviar síntomas provocados por el cáncer de esófago tales como dolor, o dificultad para tragar.Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como los pulmones, el corazón, la medula espinal, hígado, estomago, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar. Los más empleados son una máscara de material termoplástico que se adapta al contorno del paciente.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Radioterapia Interna
Esta modalidad de radioterapia en el cáncer de esófago, generalmente, se administra para mejorar la disfagia (dificultad para tragar), ya que es muy eficaz y posee pocos efectos secundarios.
Ésta se administra colocando un material radiactivo en el esófago, muy próximo al tumor, con el objetivo de administrar altas dosis de radiación a cortas distancias, de tal forma, que llega muy poca dosis a los tejidos sanos.
¿Cómo se coloca el material?
En una sonda o catéter (tubo fino y flexible) se introduce el material radiactivo. Para situarlo próximo al tumor es necesario realizar una endoscopia, que permita determinar la situación exacta del mismo. Generalmente, se emplean materiales que producen tasas de energía altas, por lo que sólo son necesarios pocos minutos para administrar la dosis, y no se hace necesario el ingreso para su aplicación. Mientras se administra es necesario que permanezca en una habitación, con paredes plomadas, preparada especialmente para tal fin.
Estará controlado, en todo momento, a través de un monitor de televisión por el personal sanitario responsable de su tratamiento.Una vez extraído el material, podrá hacer su vida normal y en ningún caso se puede considerar que emita radiación, por lo que su vida familiar, social o laboral no tiene por qué cambiar.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..Radioterapia interna
Es una técnica de tratamiento que consiste en introducir en el interior del organismo isótopos radiactivos. Se pueden implantar de forma temporal o permanente en la zona a tratar.
Con la radioterapia interna se logra administrar altas dosis de radiación a cortas distancias, de tal forma, que llega muy poca dosis a los tejidos sanos circundantes al implante.
¿Es necesario permanecer aislado?
En ocasiones, mientras tenga colocados los implantes es necesario que permanezca en una habitación, preparada especialmente para tal fin.
El paciente estará controlado, en todo momento, a través de un monitor de televisión por el personal sanitario responsable de su cuidado.
¿Cuánto dura el tratamiento? La duración del tratamiento dependerá en gran medida del tipo de isótopo que se haya empleado en el implante y de la cantidad de dosis que se quiera administrar en la zona del tumor, pero generalmente oscila entre minutos y días.¿Cómo se coloca el material?
En una sonda o catéter (tubo fino y flexible) se introduce el material radiactivo. Para situarlo próximo al tumor es necesario realizar una endoscopia, que permita determinar la situación exacta del mismo. Generalmente, se emplean materiales que producen tasas de energía altas, por lo que sólo son necesarios pocos minutos para administrar la dosis, y no se hace necesario el ingreso para su aplicación. Mientras se administra es necesario que permanezca en una habitación, con paredes plomadas, preparada especialmente para tal fin.
Estará controlado, en todo momento, a través de un monitor de televisión por el personal sanitario responsable de su tratamiento.
Una vez extraído el material, podrá hacer su vida normal y en ningún caso se puede considerar que emita radiación, por lo que su vida familiar, social o laboral no tiene por qué cambiar.
- Estómago (Cáncer)
Cáncer que se forma en los tejidos que revisten el estómago. También se llama cáncer gástrico.
La mayor parte de los tumores malignos del estómago (el 95%) derivan de las glándulas situadas en la mucosa gástrica, por lo que reciben el nombre de adenocarcinoma.
Un 50% de las veces este tumor se localiza próximo al esfínter pilórico y en un 20% aparecen en la curvatura menor.
Existen otros tumores como son los linfomas, cuya localización más frecuente dentro del tubo digestivo es el estómago, los sarcomas que se originan en la capa muscular del estómago y los tumores carcinoides. Estos últimos son mucho menos frecuentes, por lo que no van a ser considerados en este apartado.
Recientemente se han identificado un grupo de tumores del estroma parietal gástrico (GIST), cuyo pronóstico depende de distintos factores (tamaño, tipo de células…). Estos tumores son también muy infrecuentes.
Para poder determinar el tratamiento más adecuado para el cáncer gástrico, es importante clasificar el tumor, es decir, determinar en qué fase se encuentra.
El sistema que con mayor frecuencia se emplea para su clasificación es el TNM. Estas siglas hacen referencia a tres aspectos del cáncer: la T se refiere al tamaño del mismo, la N a la afectación de los ganglios linfáticos y la M a la afectación o no de otros órganos.
En función de estos aspectos, el cáncer de estómago se agrupa en las siguientes etapas o estadios:
Estadio 0 o carcinoma in situ: también conocido como carcinoma de extensión superficial. Es la fase más temprana del cáncer de estómago. Las células tumorales se encuentran situadas en la parte más superficial de la mucosa y en ningún caso la traspasan. No afecta a ganglios linfáticos.
Estadio I: el tumor afecta a toda la pared del estómago sin traspasar la serosa. En esta etapa el cáncer puede haber afectado a los ganglios linfáticos más próximos al tumor.
Estadio II: el tumor ha infiltrado la serosa sin invadir los órganos de alrededor y/o afecta a ganglios más alejados.
Estadio III: el cáncer ha invadido a los órganos más próximos y afecta a los ganglios más alejados del tumor.
Estadio IV: el cáncer se ha diseminado afectando a órganos alejados del estómago como el pulmón y/o hígado y/o huesos.
Elección del Tratamiento
Una vez que se ha confirmado el diagnóstico de cáncer de estómago y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado para curarla. El especialista le recomendará y explicará las posibilidades de tratamiento más adecuadas en su caso, para que una vez que haya recibido la suficiente información pueda, junto con su médico, tomar una decisión.
El tratamiento del cáncer de estómago, como ocurre en la mayoría de los tumores, es un tratamiento multidisciplinar. Distintas especialidades trabajan juntas para combinar terapias y ofrecer al paciente las mayores posibilidades de curación.
En el tratamiento del cáncer de estómago se sigue un protocolo, es decir un conjunto de normas y pautas (plan de tratamiento) que se establecen, basándose en la experiencia científica para el tratamiento de dicho tumor.
Estos protocolos que se emplean de forma generalizada en todos los hospitales, recogen las indicaciones o limitaciones de tratamiento en función de una serie de factores:- Fase en la que se encuentra la enfermedad (TNM)
- El tipo de célula que forma el tumor
- Edad del paciente
El médico también tendrá en cuenta, si además del cáncer de estómago, existen otras enfermedades importantes que puedan dificultar la realización de algún tratamiento específico.
El tratamiento propuesto por el especialista no va a ser el mismo en todos los pacientes.
Los tratamientos más frecuentemente empleados en el cáncer de estómago son la cirugía, la radioterapia y la quimioterapia, aunque estos dos últimos poseen un papel menos relevante en el cáncer gástrico.Estadio 0 (carcinoma in situ)
El tratamiento habitual del estadio 0 es la cirugía (gastrectomía total o subtotal).Cáncer del estómago en estadio I
El tratamiento del cáncer de estómago en estadio I puede incluir los siguientes procedimientos:
- Cirugía (gastrectomía total o subtotal).
- Cirugía (gastrectomía total o subtotal) seguida de quimiorradiación.
Cáncer del estómago en estadio II
El tratamiento del cáncer de estómago en estadio II puede incluir los siguientes procedimientos:
- Cirugía (gastrectomía total o subtotal).
- Cirugía (gastrectomía total o subtotal) seguida de quimiorradiación.
- Quimioterapia administrada antes y después de la cirugía.
Cáncer del estómago en estadio III
El tratamiento del cáncer de estómago en estadio III puede incluir los siguientes procedimientos:
- Cirugía (gastrectomía total).
- Cirugía seguida de quimiorradiación.
- Quimioterapia administrada antes y después de la cirugía.
Cáncer del estómago en estadio IVEl tratamiento del cáncer de estómago en estadio IV que no se diseminó hasta órganos distantes puede incluir los siguientes procedimientos:
- Cirugía (gastrectomía total).
- Cirugía seguida de quimiorradiación.
- Quimioterapia administrada antes y después de la cirugía.
El tratamiento del cáncer de estómago en estadio IV que se diseminó hasta órganos distantes puede incluir los siguientes procedimientos:
- Quimioterapia como terapia paliativa para aliviar síntomas y mejorar la calidad de vida.
- Terapia láser endoluminal o colocación de una cánula endoluminal para aliviar un bloqueo en el estómago.
- Radioterapia como terapia paliativa para interrumpir hemorragias, aliviar el dolor o disminuir el tamaño de un tumor que bloquea el estómago.
- Cirugía como terapia paliativa para interrumpir hemorragias o disminuir el tamaño de un tumor que bloquea el estómago.
Opciones de tratamiento para el cáncer de estómago recidivante
El tratamiento del cáncer de estómago recidivante puede incluir los siguientes procedimientos:- Quimioterapia como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
- Terapia láser endoluminal o colocación de una cánula endoluminal para aliviar un bloqueo en el estómago.
- Radioterapia como terapia paliativa para interrumpir hemorragias, aliviar el dolor o disminuir el tamaño de un tumor que bloquea el estómago.
- Cirugía como terapia paliativa para detener el sangrado o reducir el tamaño de un tumor que bloquea el estómago.
Cirugía
La cirugía suele ser el tratamiento más importante y el primero en llevarse a cabo, en la mayoría de los tumores gástricos. Con frecuencia, no es necesario complementar la cirugía con otro tratamiento para que remita la enfermedad.
El tipo de cirugía que se puede aplicar en el cáncer de estómago, varía en función del tamaño, de la localización y de la extensión de la enfermedad a ganglios y/o órganos vecinos.
La cirugía a nivel del estómago es una intervención quirúrgica mayor, por lo que es necesario un ingreso hospitalario durante un tiempo que puede variar de un enfermo a otro. Lo más habitual es que oscile entre una y dos semanas. Asimismo, es necesario anestesia que siempre será de tipo general.
La técnica más frecuente es la extirpación de parte o de la totalidad del estómago. Si el tumor afecta a una pequeña zona, en muchas ocasiones, es posible extraer todo el tumor extirpando, únicamente, una parte del estómago. Esta intervención se denomina gastrectomía parcial.
Si el tumor afecta a una zona más amplia del estómago, generalmente, es necesario extirparlo en su totalidad, gastrectomía total, para poder extraer por completo el tumor, con un margen adecuado de seguridad.
En ambas intervenciones la incisión (herida quirúrgica) se realiza en la parte anterior del abdomen, por encima del ombligo, hasta el esternón.
Independientemente de la cantidad de estómago que se necesite extirpar, se extraen los ganglios linfáticos próximos al tumor, para valorar si se ha extendido a ellos, o por el contrario, no los ha infiltrado.
Si el tumor se ha extendido localmente, es preciso extraer en la misma intervención aquellos órganos próximos al estómago que hayan sido invadidos. Por ejemplo puede ser preciso extirpar la parte baja del esófago o la primera porción del intestino delgado (duodeno).
Posteriormente, es preciso unir los extremos para poder mantener la continuidad del tubo digestivo y poder alimentarse correctamente. En el caso de una gastrectomía parcial se une el estómago restante con el intestino delgado. Si se ha extraído todo el estómago, se unirá el esófago con el duodeno.Radioterapia
En el cáncer gástrico, la radioterapia no se emplea como tratamiento exclusivo con intención curativa, ya que las dosis necesarias para destruir el tumor serían elevadas.
La radioterapia es útil en los casos en los que el tumor se ha diseminado a otros órganos y pudiera estar causando algún síntoma que disminuya la calidad de vida (radioterapia paliativa). Con dosis bajas de radiación se pueden mejorar dichos síntomas y aumentar el bienestar del paciente.
Asimismo, se puede emplear asociada a la quimioterapia tras la cirugía para eliminar las células que no se han podido extirpar. En este caso la dosis de radiación tampoco debe alcanzar dosis que pudieran lesionar los órganos más sensibles próximos al tumor.
El tratamiento con radioterapia siempre es individualizado, es decir, cada enfermo tendrá su tratamiento específico y distinto al de otro paciente.Quimioterapia
Los tumores malignos se caracterizan por estar formados por células transformadas cuyos mecanismos que regulan la división se han alterado, por lo que son capaces de dividirse descontroladamente e invadir y afectar órganos vecinos.
La mayoría de los fármacos que se emplean en el tratamiento quimioterápico están diseñados para poder destruir las células mientras se dividen. Cuanto más rápido se dividen más sensibles son al tratamiento.
Con el tiempo esto se traduce en una disminución o desaparición del tumor maligno.
En algunos casos, en los que el cáncer gástrico no se ha diseminado a otros órganos, pero no es posible operarlo por su extensión local, la quimioterapia puede reducir dicho tumor y facilitar la cirugía posterior.
Asimismo, se puede emplear tras la cirugía asociada a la radioterapia (sin que esta supere una dosis determinada, para no lesionar otras estructuras). El objetivo es eliminar las células que hayan podido quedar en la zona de la cirugía y que no son visibles.
Con frecuencia, la quimioterapia se emplea en aquellos tumores que se han extendido a otros órganos, se utiliza como tratamiento único y su objetivo, fundamental, es disminuir los síntomas derivados del tumor y mejorar la calidad de vida del paciente.-
H
- Higado (Cáncer)
- El cáncer primario de hígado es cáncer que se forma en los tejidos del hígado. El cáncer secundario del hígado es cáncer que se disemina al hígado desde otra parte del cuerpo. Cuando las células tumorales, con capacidad de invadir los tejidos sanos de alrededor y de alcanzar órganos alejados e implantarse en ellos, están ubicadas en el hígado, hablamos de cáncer de hígado o hepatocarcinoma.
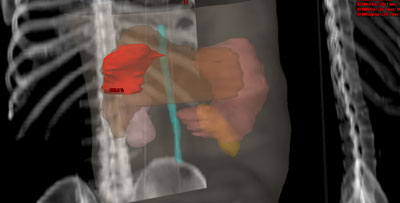
El carcinoma hepatocelular es un tumor relativamente importante en España: se diagnostican más de 3.000 casos anuales en nuestro país (14 por cada 100.000 hombres y 4 por cada 100.000 mujeres, anualmente). Además, es el cáncer más frecuente en otros países, particularmente en aquellos que tienen mayor incidencia de infección por el virus de la hepatitis C.
En el resto del mundo, el cáncer de hígado representa un problema de salud, con más de un millón de casos diagnosticados cada año en todo el mundo
El cáncer de hígado se puede curar si el tumor se extirpa mediante una intervención quirúrgica. Los pacientes candidatos a cirugía requieren una evaluación preoperatoria muy detallada incluyendo la realización estudios radiológicos con el TAC, la RMN o la angiografía.
Antes de la intervención se puede realizar un estudio con laparosocopia para descartar que hubiera contraindicación para la resección quirúrgica, por ejemplo porque hubiera metástasis.
Sin embargo no siempre es posible la intervención quirúrgica. En estos casos existen tratamientos disponibles, como la quimioterapia intraarterial (también denominada quimioembolización), inyección percutánea de etanol, ablación con radiofrecuencia, crioterapia o la quimioterapia sistémica.
Se utilizan los siguientes estadios para el cáncer primario de hígado en adultos:Estadio IEn el estadio I, hay un tumor que no se diseminó hasta los vasos sanguíneos cercanos.
Estadio IIEn el estadio II, se encuentra uno de los siguientes casos:- Hay un tumor que se diseminó hasta los vasos sanguíneos; o cercanos.
- Hay más de un tumor y ninguno mide más de cinco centímetros.
Estadio IIIEl estadio III se subdivide en estadio IIIA, IIIB y IIIC.- En el estadio IIIA, se encuentra uno de los siguientes casos:
- Hay más de un tumor que mide más de cinco centímetros.
- Hay un tumor que se diseminó hasta una rama principal de vasos sanguíneos cercanos al del hígado.
En el estadio IIIB, hay uno o más tumores de cualquier tamaño que:- Se diseminaron hasta los órganos cercanos, pero no a la vesícula biliar.
- Atravesaron el revestimiento de la cavidad peritoneal.
En el estadio IIIC, el cáncer se diseminó hasta los ganglios linfáticos cercanos.Estadio IVEn el estadio IV, el cáncer se diseminó más allá del hígado hasta otros lugares del cuerpo, como los huesos o los pulmones. Los tumores pueden ser de cualquier tamaño y también pueden haberse diseminado hasta los vasos sanguíneos o los ganglios linfáticos cercanos.
El cáncer primario de hígado en adultos también se agrupa según el modo en que se puede tratar el cáncer. Hay tres grupos de tratamiento:
Localizado resecable
El cáncer se encuentra solamente en el hígado, no se diseminó y se puede extirpar completamente con cirugía.
Localizado y localmente avanzado no resecable
El cáncer se encuentra solamente en el hígado y no se diseminó, pero no se puede extirpar completamente con cirugía.
Avanzado
El cáncer se diseminó por todo el hígado o hasta otras partes del cuerpo, como los pulmones y los huesos.
Opciones de tratamiento
Cáncer primario del hígado en adultos localizado resecable
El tratamiento del cáncer primario de hígado en adultos localizado resecable puede incluir los siguientes procedimientos:- Cirugía (hepatectomía parcial).
- Cirugía (hepatectomía total) y trasplante de hígado.
- Participación en un ensayo clínico de quimioterapia regional o quimioterapia sistémica, o terapia biológica después de la cirugía.
Cáncer primario de hígado en adultos localizado y localmente avanzado no resecable
El tratamiento del cáncer primario de hígado en adultos localizado y localmente avanzado no resecable puede incluir los siguientes procedimientos:- Cirugía (criocirugía o ablación por radiofrecuencia).
- Quimioterapia (quimioembolización, quimioterapia regional o quimioterapia sistémica).
- Inyección percutánea de etanol.
- Cirugía (hepatectomía total) y trasplante de hígado.
- Radioterapia con radiosensibilizadores.
- Participación en un ensayo clínico de una combinación de cirugía, quimioterapia y radioterapia. También se puede utilizar terapia de hipertermia. Se puede utilizar la quimioterapia y la radioterapia para reducir el tumor antes de la cirugía.
Cáncer primario de hígado en adultos avanzadoNo hay un tratamiento estándar para el cáncer primario de hígado en adultos avanzado. Los pacientes pueden considerar participar en un ensayo clínico.El tratamiento puede ser un ensayo clínico de terapia biológica, quimioterapia o radioterapia con radiosensibilizadores o sin ellos.Estos tratamientos se pueden administrar como terapia paliativa para ayudar a aliviar los síntomas y mejorar la calidad de vida.
Cáncer primario de hígado en adultos recidivanteEl tratamiento del cáncer primario de hígado en adultos recidivante puede incluir los siguientes procedimientos:- Cirugía (hepatectomía parcial).
- Cirugía (hepatectomía total) y trasplante de hígado.
- Quimioterapia (quimioembolización o quimioterapia sistémica).
- Inyección percutánea de etanol.
- Participación en un ensayo clínico de un tratamiento nuevo.
Cirugía
Para tratar el cáncer de hígado, se pueden utilizar los siguientes tipos de cirugía:
- Criocirugía: tratamiento para el que se utiliza un instrumento para congelar y destruir tejido anormal, como carcinoma in situ. Este tipo de tratamiento también se llama crioterapia. El médico puede utilizar una sonda de ecografía para guiar el instrumento.
- Hepatectomía parcial: extirpación de la parte del hígado donde se encuentra el cáncer. La parte extirpada puede ser una cuña de tejido, un lóbulo completo o una porción más grande del hígado, junto con parte del tejido sano que la rodea. El tejido hepático restante se hace cargo de las funciones del hígado.
- Hepatectomía total y trasplante de hígado: extirpación de todo el hígado y reemplazo con un hígado donado sano. Se puede realizar un trasplante de hígado cuando la enfermedad se localiza en el hígado solamente y se puede encontrar un hígado donado. Si el paciente debe esperar para recibir un hígado donado, se administra otro tratamiento de acuerdo con la necesidad.
- Ablación por radiofrecuencia: uso de una sonda especial con electrodos pequeños que destruyen células cancerosas. Algunas veces la sonda se introduce directamente a través de la piel y solo se necesita anestesia local. En otros casos, la sonda se introduce a través de una incisión en el abdomen. Esto se realiza en el hospital con anestesia general.
Quimioterapia
La quimioterapia es un tratamiento de cáncer que utiliza medicamentos para interrumpir el crecimiento de las células cancerosas, mediante su destrucción o impidiendo su multiplicación. Cuando la quimioterapia se administra oralmente o se inyecta en una vena o músculo, los medicamentos ingresan al torrente sanguíneo y afectan a células cancerosas de todo el cuerpo (quimioterapia sistémica).
Cuando la quimioterapia se coloca directamente en la columna espinal, un órgano o una cavidad corporal como el abdomen, los medicamentos afectan principalmente células cancerosas en esas áreas (quimioterapia regional).
La quimioterapia regional se suele utilizar para tratar el cáncer de hígado. Se puede colocar en el cuerpo una bomba pequeña que contiene medicamentos contra el cáncer. La bomba envía los medicamentos directamente hasta vasos sanguíneos que van al tumor.
Otro tipo de quimioterapia regional es la quimioembolización de la arteria hepática. El medicamento contra el cáncer se inyecta en la arteria hepática a través de un catéter (tubo delgado). El medicamento se combina con una sustancia que bloquea la arteria y corta el flujo de sangre hacia el tumor.
La mayor parte del medicamento contra el cáncer queda atrapada cerca del tumor y solo una pequeña cantidad llega a otras partes del cuerpo. El bloqueo puede ser temporal o permanente, según la sustancia que se utiliza para bloquear la arteria. Se impide que el tumor reciba el oxígeno y los nutrientes que necesita para crecer.
El hígado continúa recibiendo sangre de la vena porta hepática, que lleva la sangre del estómago y el intestino.
La forma en que se administra la quimioterapia depende del tipo y el estadio del cáncer que se está tratando.
Radioterapia
La radioterapia es un tratamiento de cáncer que utiliza rayos X de alta energía u otros tipos de radiación para destruir células cancerosas o impedir que crezcan. La radioterapia se administra de diferentes modos:
- La radioterapia externa utiliza una máquina fuera del cuerpo que envía radiación hacia el cáncer.
- Se pueden administrar medicamentos que se llaman radiosensibilizadores junto con la radioterapia para lograr que las células se vuelvan más sensibles a la radioterapia.
- La radioterapia se puede administrar al tumor junto con unos anticuerpos radiomarcados conocidos como radiosensibilizadores. Las sustancias radiactivas se unen a los anticuerpos producidos en el laboratorio. Estos anticuerpos, que se dirigen a las células tumorales, se inyectan en el cuerpo y las células cancerosas se destruyen con la sustancia radiactiva.
La forma en que se administra la radioterapia depende del tipo y el estadio del cáncer que se está tratando.
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo.
Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como el estomago, el páncreas, la medula espinal, entre otros.Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.Los más empleados son una máscara de material termoplástico que se adapta al contorno del paciente.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres.Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos.Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad.Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona.En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..
-
L
- Laringe (Cáncer)
Cáncer que se forma en los tejidos de la laringe (parte de la garganta que contiene las cuerdas vocales y que se usa para respirar y hablar).
Las formas más comunes de cáncer de laringe reciben nombres que dependen del tipo de célula del que se derivan.
La mucosa de la laringe está formada por células planas llamadas escamosas, por lo que el tumor derivado de ellas se denominará carcinoma escamoso o epidermoide (estas células recuerdan a las de la piel o epidermis). Es el tipo de cáncer más frecuente en esta localización.
Pero, por otra parte, los cánceres de laringe se clasifican según la zona del órgano en la que se originen. Por esto, se habla de cáncer supraglótico, glótico o subglótico según donde esté localizado.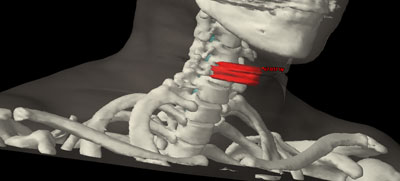
Para poder indicar el tratamiento más adecuado para el cáncer de laringe, es importante "clasificar" el tumor, es decir, determinar en qué fase se encuentra.
El sistema que con mayor frecuencia se emplea para su clasificación es el TNM. Estas siglas hacen referencia a 3 aspectos del cáncer: la T se refiere al tamaño del mismo, la N a la afectación de los ganglios linfáticos y la M a la afectación o no de otros órganos.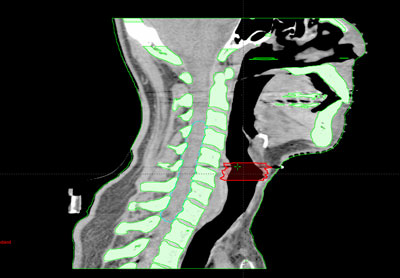
En función de estos aspectos, el cáncer de laringe se agrupa en las siguientes etapas o estadios:
Estadio 0 ó carcinoma in situ: es la fase más temprana del cáncer de laringe. Las células tumorales se encuentran situadas en la parte más superficial de la mucosa y en ningún caso la traspasa. No afecta a ganglios linfáticos.
Estadio I: el tumor afecta a la mucosa, pero sólo se encuentra en una de las regiones de la laringe, no extendiéndose a ninguna otra de las partes de dicho órgano. En esta etapa el cáncer no afecta a los ganglios linfáticos ni a ningún otro órgano.
Estadio II: el tumor afecta a varias de las zonas de la laringe (supraglotis y cuerda vocal, o glotis y subglotis). En esta etapa el cáncer no afecta a los ganglios linfáticos ni a ningún otro órgano.
Estadio III: el cáncer está limitado a la laringe con cuerdas vocales fijas (no invade órganos cercanos), aunque puede haber afectado a un ganglio linfático de la zona de origen inicial.
Estadio IV: el cáncer se ha extendido, afectando al cartílago tiroides o estructuras cercanas (boca o tejidos del cuello); o bien tiene infiltración por vía linfática de forma importante; o presenta diseminación a distancia (afecta a pulmón, hígado, huesos o a ganglios linfáticos alejados de la zona del tumor).
El grado celular es importante a la hora de decidir un tratamiento. Las células tumorales se clasifican en G1/G2/G3 en función de su potencial agresividad (de menor a mayor agresividad).
Elección del TratamientoUna vez que se ha confirmado el diagnóstico de cáncer de laringe y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más apropiado. El especialista le recomendará y explicará las posibilidades de tratamiento más adecuadas en su caso, para que una vez que haya recibido la suficiente información pueda, junto con su médico tomar una decisión.
El tratamiento del cáncer de laringe, como ocurre en la mayoría de los tumores, es un tratamiento multidisciplinar. Distintas especialidades trabajan juntas para combinar terapias y ofrecer al paciente las mayores posibilidades de curación.
El plan de tratamiento del cáncer de laringe se basa en una serie de normas y pautas (protocolo), establecidas por cada hospital basándose en la experiencia clínica.
Estos protocolos, que se emplean de forma generalizada en todos los hospitales, recogen las indicaciones o limitaciones de tratamiento en función de una serie de factores:- Estadio en el que se encuentra la enfermedad (TNM).
- La localización del cáncer: el tratamiento puede variar dependiendo de si la enfermedad está localizada en la región supraglótica, glotis o cuerdas vocales, o región subglótica.
- Grado celular.
Probablemente, el médico también tendrá en cuenta, si además del cáncer de laringe, existen otras enfermedades importantes que puedan dificultar la realización de algún tratamiento específico.
Por tanto el tratamiento propuesto por el especialista no va a ser el mismo en todos los pacientes.
Los tratamientos más frecuentemente empleados en el cáncer de laringe son, fundamentalmente, la cirugía, la radioterapia y la quimioterapia.
En los siguientes apartados se describen cada una de ellos tratando de explicar en qué consisten, qué efectos adversos producen y cuáles son las recomendaciones para minimizar dichos efectos.
Cáncer de la laringe en estadio I
El tratamiento del cáncer de la laringe en estadio I depende de la ubicación del cáncer en la laringe.
Si el cáncer está en la supraglotis, el tratamiento puede incluir los siguientes procedimientos:- Radioterapia.
- Laringectomía supraglótica.
Si el cáncer está en la glotis, el tratamiento puede incluir los siguientes procedimientos:
- Radioterapia.
- Cordectomía.
- Laringectomía parcial, hemilaringectomía o laringectomía total.
- Cirugía láser.
Si el cáncer está en la subglotis, el tratamiento puede incluir los siguientes procedimientos:- Radioterapia, con cirugía o sin esta.
- Cirugía sola.
Cáncer de la laringe en estadio II
El tratamiento para el cáncer de la laringe en estadio II depende de la ubicación del cáncer en la laringe.
Si el cáncer está en la supraglotis, el tratamiento puede incluir los siguientes procedimientos:- Radioterapia.
- Laringectomía supraglótica o laringectomía total, con radioterapia o sin esta.
Si el cáncer está en la glotis, el tratamiento puede incluir los siguientes procedimientos:
- Radioterapia.
- Laringectomía parcial, hemilaringectomía o laringectomía total.
- Cirugía láser.
Si el cáncer está en la subglotis, el tratamiento puede incluir los siguientes procedimientos:
- Radioterapia, con cirugía o sin esta.
- Cirugía sola.
Cáncer de la laringe en estadio III
El tratamiento para el cáncer de la laringe en estadio III depende de la ubicación del cáncer en la laringe.
Si el cáncer está en la supraglotis o glotis, el tratamiento puede incluir los siguientes procedimientos:- Cirugía, con radioterapia o sin esta.
- Radioterapia, con cirugía o sin esta.
Si el cáncer está en la subglotis, el tratamiento puede incluir los siguientes procedimientos:
- Laringectomía más tiroidectomía total y extracción de los ganglios linfáticos de la garganta, habitualmente seguida de radioterapia.
- Radioterapia, con cirugía o sin esta.
Cáncer de la laringe en estadio IV
El tratamiento para el cáncer de la laringe en estadio IV depende de la ubicación del cáncer en la laringe.
Si el cáncer está en la supraglotis o la glotis, el tratamiento puede incluir los siguientes procedimientos:- Laringectomía total, con radioterapia.
- Radioterapia, con cirugía o sin esta.
Si el cáncer está en la subglotis, el tratamiento puede incluir los siguientes procedimientos:
- Laringectomía más tiroidectomía total y extracción de los ganglios linfáticos de la garganta, generalmente con radioterapia.
- Radioterapia.
Opciones de tratamiento para el cáncer de la laringe recidivante
El tratamiento para el cáncer de la laringe recidivante puede incluir los siguientes procedimientos:- Cirugía, con radioterapia o sin esta.
- Radioterapia.
- Quimioterapia.
Quimioterapia
En el cáncer de laringe, la quimioterapia se aplica, generalmente, asociada a la radioterapia para potenciar el efecto de esta última sobre el tumor. Al administrar ambos tratamientos, es frecuente que aumenten los efectos secundarios.
Puede administrarse antes de la cirugía o radioterapia, para disminuir el tamaño del tumor y facilitar el tratamiento local o después de la cirugía o radioterapia para prevenir la reaparición de la enfermedad.
Si el tumor está muy diseminado y no responde a otros tratamientos, la quimioterapia puede utilizarse como tratamiento paliativo. Su objetivo fundamental es disminuir los síntomas derivados del tumor y mejorar la calidad de vida del paciente.
Unida a la Radioterapia, se emplea en ocasiones para evitar realizar una laringectomía.Cirugía
El tipo de cirugía que se puede aplicar en el cáncer de laringe varía en función del tamaño, de la localización y de la extensión de la enfermedad a ganglios y/o órganos vecinos.
La cirugía a nivel de laringe es una intervención quirúrgica mayor, por lo que es necesario un ingreso hospitalario durante un tiempo que puede variar de un enfermo a otro, pero por lo general suele oscilar entre una y dos semanas. Asimismo, es necesaria anestesia, que siempre será de tipo general.
Aunque es posible que se tenga que realizar la extirpación de la laringe (laringectomía), en la actualidad se realizan con más frecuencia cirugías conservadoras para preservar la voz.
Dependiendo de la situación de cada enfermo, existen diferentes opciones y técnicas de tratamiento quirúrgico:- Laringectomía total: cuando se precisa extirpar toda la laringe.
- Cordectomía: consiste en la extirpación únicamente de la cuerda vocal afecta.
- Laringectomía supraglótica: se extirpa solamente la región supraglótica de la laringe.
- Linfadenectomía: es la extirpación de los ganglios linfáticos de la zona del cuello. Dependiendo de la localización del tumor, el riesgo de afectación de los ganglios del cuello puede variar. En los tumores supra y subglóticos es frecuente esta afectación por lo que se suele llevar a cabo la linfedenectomía. Se conoce con el nombre de disección ganglionar cervical.
En los cánceres de glotis, no se afectan los ganglios por lo que no es preciso realizar este tipo de cirugía.
Radioterapia
La radioterapia es el empleo de radiaciones ionizantes para el tratamiento, local o locorregional, de determinados tumores que emplea rayos X con altas dosis de irradiación.
Su objetivo es destruir las células tumorales causando el menor daño posible a los tejidos sanos que rodean dicho tumor.
En la mayoría de los tumores, la radioterapia que se aplica es externa. Para ello se emplean máquinas de gran tamaño que, en ningún momento contactan con el enfermo.
La radioterapia se puede emplear como tratamiento único o en combinación. Se puede administrar antes de la intervención para disminuir su tamaño y facilitar la cirugía, o después de la misma, para consolidar el tratamiento.
Asimismo, se puede administrar con la quimioterapia para potenciar sus efectos (quimioirradiación).
El tratamiento con radioterapia siempre es individualizado, es decir, cada enfermo tendrá su tratamiento específico y distinto al de otro paciente, dependiendo de la localización y extensión de la enfermedad.
Según la finalidad con que se emplee, la radioterapia puede ser curativa o paliativa.
Dependiendo de la localización, y sobre todo de la fase en la que se encuentre la enfermedad, puede ser un tratamiento con finalidad curativa, sobre todo en etapas iniciales. Suele dar buenos resultados para los cánceres localizados en la glotis.
Salvo para los tumores de glotis, suele ser necesario casi siempre que el tratamiento comprenda todo el cuello.
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como la medula espinal, las glándulas parótidas, la cavidad oral, la orofaringe, la traquea, el esófago, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar. Los más empleados son una máscara de material termoplástico que se adapta al contorno del paciente.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control.
-
M
- Mama (Cáncer)
Cáncer que se forma en los tejidos de la mama, por lo general en los conductos (tubos que llevan leche al pezón) y los lobulillos (glándulas que producen leche).
Se puede presentar tanto en los hombres como en las mujeres, aunque el cáncer de mama masculino es raro.
El cáncer de mama es el tumor más frecuente en las mujeres occidentales.
Gracias a los programas de detección precoz y a los avances en el diagnóstico y tratamiento cada día es mayor el número de mujeres que viven con el cáncer de mama y lo superan.
El cáncer de mama es el tumor maligno que se origina en el tejido de la glándula mamaria.
Cuando las células tumorales con capacidad de invadir los tejidos sanos de alrededor y de alcanzar órganos alejados e implantarse en ellos, están ubicadas en la mama, hablamos de cáncer de mama.
Pero el cáncer de mama no es una enfermedad exclusiva de mujeres, aunque en un porcentaje muy pequeño, los hombres también pueden padecerlo ver capítulo cáncer de mama en el varón.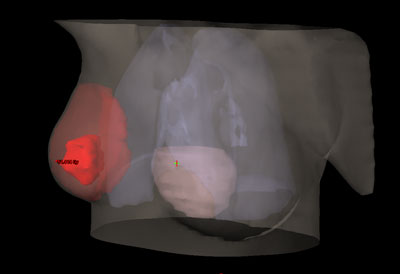
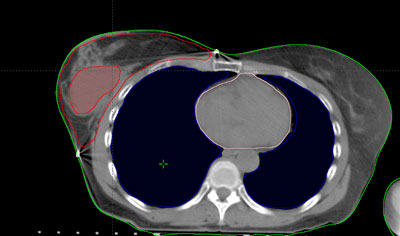
Elección de tratamiento
Una vez que se ha confirmado el diagnóstico de cáncer de mama y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado para tí.
El especialista recomendará y explicará las posibilidades del tratamiento más adecuadas en cada caso, para que una vez que la paciente haya recibido la suficiente información pueda, junto con el médico, tomar una decisión.
El tratamiento del cáncer de mama, como ocurre en la mayoría de los tumores, es multidisciplinar. Distintas especialidades trabajan juntas para combinar terapias y ofrecer al paciente las mayores posibilidades de curación.
En el cáncer de mama se utilizan diversos tipos de tratamientos: cirugía, radioterapia, quimioterapia, hormonoterapia, anticuerpos monoclonales. Estos tratamientos se combinan en función de las características del tumor en cada paciente.
En el tratamiento del cáncer de mama se sigue un protocolo, es decir un conjunto de normas y pautas (plan de tratamiento), establecidas en base a la experiencia científica que se tiene en el tratamiento de este tumor.
Estos protocolos, que se emplean de forma generalizada en todos los hospitales, recogen las indicaciones o limitaciones del tratamiento en función de los siguientes factores:
- Edad del paciente
- Estado general
- Estado hormonal (premenopausia, menopausia)
- Localización del tumor
- Fase o estadio en la que se encuentra la enfermedad (TNM)
- Receptores hormonales del tumor
- Grado de las células
- Positividad para algunos factores biológicos (por ejemplo Her2)
Probablemente, el médico también tendrá en cuenta si además del cáncer de mama, existen otras enfermedades importantes que puedan dificultar la realización de algún tratamiento específico. Por tanto, el tratamiento propuesto por el especialista no va a ser el mismo en todos los pacientes.
Se utilizan diversas definiciones respecto al tratamiento:- Tratamiento Local: Se refiere al tratamiento dirigido al tumor en su lugar de origen o en alguna localización determinada. La cirugía y la radioterapia son ejemplos de ello.
- Tratamiento Sistémico: Se refiere al tratamiento que afecta a todo el organismo. La quimioterapia y la hormonoterapia son tratamientos sistémicos.
- Tratamiento Adyuvante: Se llama así al tratamiento sistémico administrado tras un tratamiento local sin que exista evidencia de enfermedad. El objetivo de este tratamiento es destruir células tumorales que estén dispersas por el organismo.
- Tratamiento Neoadyuvante: Consiste en administrar un tratamiento sistémico antes de un tratamiento local, con el objetivo de reducir el tamaño del tumor antes de la cirugía.
Carcinoma ductal in situ (CDIS)
El tratamiento del carcinoma ductal in situ (CDIS) puede incluir los siguientes procedimientos:
- Cirugía para preservar la mama y radioterapia, con tamoxifeno o sin este.
- Mastectomía total, con tamoxifeno o sin este.
- Cirugía para preservar la mama, sin radioterapia.
Carcinoma lobular in situ (CLIS)
El tratamiento del carcinoma lobular in situ (CLIS) puede incluir los siguientes procedimientos:
- Biopsia para diagnosticar el CLIS seguida de exámenes regulares y mamogramas regulares a fin de detectar cambios tan pronto como sea posible. Esto se llama observación.
- Tamoxifeno para reducir el riesgo de padecer de cáncer de mama.
- Mastectomía profiláctica bilateral. Esta opción de tratamiento se usa a veces para mujeres que tienen un riesgo alto de padecer de cáncer de mama. La mayoría de los cirujanos cree que en estos casos es un tratamiento más radical que el que se necesita.
Cáncer de mama en estadios I, II, IIIA y IIIC operable
El tratamiento de los estadios I, II, IIIA y IIIC operables puede incluir los siguientes procedimientos:
- Cirugía para preservar la mama para extirpar solo el cáncer y parte del tejido que rodea la mama, seguida por disección de ganglios linfáticos y radioterapia.
- Mastectomía radical modificada con cirugía para la reconstrucción de la mama o sin ella.
La terapia adyuvante (tratamiento suministrado después de la cirugía para aumentar la probabilidad de curación) puede incluir los siguientes procedimientos:
- Radioterapia dirigida a los ganglios linfáticos cerca de la mama y la pared torácica después de una mastectomía radical modificada.
- Quimioterapia sistémica, con terapia con hormonas o sin esta.
- Terapia con hormonas.
Cáncer de mama en estadio IIIB, estadio IIIC inoperable, estadio IV y metastásico
Cáncer de mama en estadio IIIB y estadio IIIC inoperable
El tratamiento del estadio IIIB y el estadio IIIC inoperable del cáncer de mama puede incluir los siguientes procedimientos:- Quimioterapia sistémica.
- Quimioterapia sistémica seguida de cirugía (cirugía para preservar la mama o mastectomía total), con disección de ganglios linfáticos seguida de radioterapia. Se puede administrar terapia sistémica adicional (quimioterapia, terapia con hormonas o ambas).
Cáncer de mama en estadio IV y metastásico
El tratamiento del cáncer de mama en estadio IV o el cáncer de mama metastásico puede incluir los siguientes procedimientos:
- Terapia con hormonas o quimioterapia sistémica con trastuzumab (Herceptina) o sin este.
- Terapia con inhibidores de la tirosina cinasa con lapatinib, combinado con capecitabina.
- Radioterapia o cirugía para el aliviar el dolor y otros síntomas.
- Medicamentos con bisfosfonato para reducir la enfermedad de los huesos y el dolor cuando el cáncer se diseminó hasta el hueso.
Opciones de tratamiento para el cáncer de mama inflamatorio
El tratamiento del cáncer de mama inflamatorio puede incluir los siguientes procedimientos:
- Quimioterapia sistémica.
- Quimioterapia sistémica seguida de cirugía (cirugía para preservar la mama o mastectomía total), con disección de ganglios linfáticos seguida de radioterapia. Se puede administrar terapia sistémica adicional (quimioterapia, terapia con hormonas o ambas).
Opciones de tratamiento para cáncer de mama recidivante
El tratamiento del cáncer de mama recidivante (cáncer que volvió después de terminar el tratamiento) en la mama o la pared del pecho puede incluir los siguientes procedimientos:
- Cirugía (mastectomía radical o mastectomía radical modificada), radioterapia o ambas.
- Quimioterapia sistémica o terapia con hormonas.
Opciones de tratamiento para el cáncer de seno (mama) masculino
El cáncer de mama masculino se trata del mismo modo que el cáncer de mama en las mujeres.
Cirugía inicial
El tratamiento de los hombres con diagnóstico de cáncer de mama es habitualmente una mastectomía radical modificada. Para algunos hombres, se puede usar la cirugía para preservar la mama con tumorectomía.
Terapia adyuvante
El tratamiento administrado después de una operación cuando ya no es posible ver células cancerosas se llama terapia adyuvante. Incluso si el médico extirpa todo el cáncer que se puede ver en el momento de la operación, es posible que el paciente reciba radioterapia, quimioterapia, terapia con hormonas o terapia dirigida después de la cirugía para tratar de destruir toda célula cancerosa que pueda haber quedado.
- Ganglios linfáticos negativos: para los hombres cuyo cáncer es de ganglios linfáticos negativos (el cáncer no se diseminó hasta los ganglios linfáticos), se debe considerar la terapia coadyuvante sobre la misma base que para las mujeres con cáncer de mama porque no hay datos contundentes de que la respuesta al tratamiento es diferente para los hombres que para las mujeres.
- Ganglios linfático positivos: para hombres que padecen cáncer con ganglios linfáticos positivos (el cáncer no se diseminó hasta los ganglios linfáticos), la terapia adyuvante puede incluir los siguientes procedimientos:
- Quimioterapia más tamoxifeno (para bloquear el efecto del estrógeno).
- Otra terapia con hormonas.
- Participación en un ensayo clínico de terapia dirigida con un anticuerpo monoclonal (trastuzumab).
Estos tratamientos parecen aumentar la supervivencia de los hombres así como de las mujeres. La respuesta de los pacientes a la terapia hormonal depende de que haya receptores hormonales (proteínas) en el tumor. La mayoría de los cánceres de mama en los hombres tienen estos receptores.
La terapia con hormonas habitualmente se recomienda para pacientes varones con cáncer de mama, pero puede tener muchos efectos secundarios, incluso sofocos e impotencia (la incapacidad de lograr una erección adecuada para mantener relaciones sexuales).
Metástasis a distancia
El tratamiento de los hombres con metástasis a distancia (cáncer que se diseminó hasta otras partes del cuerpo) puede ser terapia con hormonas, quimioterapia o ambas. La terapia con hormonas puede incluir los siguientes procedimientos:
- Orquiectomía (extirpación de los testículos para disminuir la producción de hormonas).
- Agonista de la hormona liberadora de hormona luteinizante, con o sin bloqueo total de andrógenos (para disminuir la producción de hormonas sexuales).
- Tamoxifeno para cáncer que tiene receptores de estrógeno positivos.
- Progesterona (una hormona femenina).
- Inhibidores de la aromatasa (para disminuir la cantidad de estrógeno elaborado).
Los tratamientos hormonales pueden emplearse en secuencia (una después de la otra). Se pueden utilizar regímenes de quimioterapia estándar si la terapia con hormonas no es efectiva. Los hombres habitualmente responden a la terapia de la misma manera que las mujeres que padecen de cáncer de mama.
Cáncer de mama masculino recidivante
Para los hombres con la enfermedad que recidiva localmente (cáncer que volvió a un área limitada después del tratamiento), el tratamiento habitualmente es uno de los siguientes procedimientos:
- Cirugía combinada con quimioterapia; o
- Radioterapia combinada con quimioterapia.
Quimioterapia
La quimioterapia es una de las modalidades terapéuticas más empleada en el tratamiento del cáncer. Su objetivo es destruir, empleando una gran variedad de fármacos, las células que componen el tumor con el fin de lograr la reducción o desaparición de la enfermedad.
A los fármacos empleados en este tipo de tratamiento se les denomina fármacos antineoplásicos o quimioterápicos.
Estos fármacos llegan a prácticamente todos los tejidos del organismo y ahí es donde ejercen su acción, tanto sobre las células malignas como sobre las sanas. Debido a la acción de los medicamentos sobre éstas últimas, pueden aparecer una serie de síntomas más o menos intensos y generalmente transitorios, denominados efectos secundarios.
Hormonoterapia
Consiste en la administración, generalmente por vía oral, de hormonas que bloquean la acción de los estrógenos sobre las células malignas de la mama, impidiendo su proliferación, por lo que el tumor puede disminuir de tamaño o incluso desaparecer.
Existen diversos fármacos disponibles hoy día. El más conocido es el Tamoxifeno. Más novedosos son los Inhibidores de la Aromatasa (enzima que participa en la síntesis de estrógenos, especialmente en la mujeres postmenopáusicas) como el Anastrozol, Letrozol y Examestano.
Los tumores que tienen receptores hormonales positivos son los que pueden ser tratados con hormonoterapia. La elección de cada fármaco dependerá de muchos factores que tu médico tendrá en cuenta.
La duración de la hormonoterapia, cuando se utiliza como tratamiento complementario, suele ser prolongada, de, al menos, cinco años.Otros fármacos hormonales utilizados en el cáncer de mama son los antiestrógenos puros (Fulvestrant, Toremifeno). Para las pacientes premenopáusicas existen fármacos que producen una castración química como el Goserelin y el Leuprolide. Por último también existen fármacos derivados de la progesterona, otra hormona femenina.
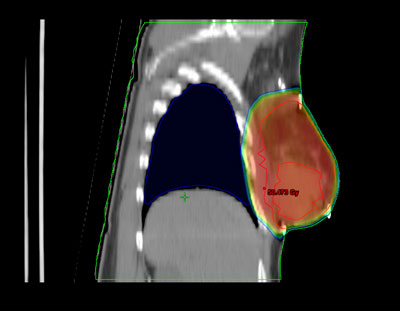
Cirugía
La cirugía a nivel de la mama es una intervención quirúrgica mayor, por lo que es necesario un ingreso hospitalario durante un tiempo que puede variar de un enfermo a otro, pero por lo general suele ser de una semana. Asimismo, es necesaria una anestesia, que siempre será de tipo general.
Antes de la intervención, es preciso realizar un estudio denominado estudio preoperatorio que consiste, generalmente, en un análisis de sangre y de coagulación, un electrocardiograma y una radiografía de tórax.
Previamente a la cirugía, debes preguntar y recibir toda la información sobre la técnica quirúrgica mediante la cual vas a ser intervenida, los riesgos y complicaciones que conlleva la intervención, las secuelas que pueden permanecer y las recomendaciones adecuadas para minimizar dichas complicaciones.
En la actualidad, los pacientes deben firmar un documento, llamado consentimiento informado, donde consta, por escrito, toda la información aportada por el especialista. En él reconocen haber recibido y comprendido la información expuesta y aceptan recibir dicho tratamiento. Es conveniente estar seguros antes de firmar dicho documento y recibir el tratamiento.Radioterapia
Su objetivo es destruir las células tumorales causando el menor daño posible a los tejidos sanos que rodean a dicho tumor.
La radioterapia se emplea generalmente tras la intervención quirúrgica para "limpiar" la zona de la cirugía de las posibles células tumorales que hayan podido quedar.En el caso de cirugía conservadora, la aplicación de la radioterapia tras la intervención es imprescindible.
Según la finalidad con que se emplee, la radioterapia puede ser curativa o paliativa para aliviar síntomas provocados por el cáncer de mama o las metástasis. Este es el caso de la radioterapia antiálgica, utilizada en las lesiones óseas con el fin de disminuir el dolor que producen al paciente.En el cáncer de mama se utiliza tanto la radioterapia externa como la interna, aunque la más frecuente es la externa. En cualquier caso es el oncólogo radioterapeuta quien prescribe y planifica el tratamiento con radioterapia.
El tratamiento con radioterapia siempre es individualizado, es decir, cada enfermo tendrá su tratamiento específico y distinto al de otro paciente.
La radioterapia externa es el tipo de radioterapia más común. La radiación procede de una fuente que se encuentra fuera del organismo.
Radioterapia interna o braquiterapia
La radioterapia interna se administra colocando un material radiactivo (isótopo) en forma de aguja (implantes), en el tumor o la zona donde estuvo situado, con el objetivo de administrar altas dosis de radiación a cortas distancias, de tal forma, que llega muy poca dosis a los tejidos sanos.
En el cáncer de mama este tipo de técnica se suele emplear, fundamentalmente, tras la cirugía conservadora, para dar en la zona del tumor más dosis de radiación (sobreimpresión). La colocación del material radiactivo se hace con anestesia general.
Mientras se tengan colocados los implantes es necesario permanecer en una habitación con paredes plomadas, preparada especialmente para tal fin, ya que las fuentes radiactivas implantadas son emisoras de radiación. L
a duración del tratamiento es de varios días. Estarás controlada y en comunicación, en todo momento, a través de un monitor de televisión y un micrófono con el personal sanitario responsable de tu tratamiento.
Una vez extraído el material podrás hacer tu vida normal, ya que no emite ningún tipo de radiación por lo que tu vida familiar, social o laboral no tiene por qué cambiar.
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como los pulmones, el corazón, la medula espinal, la mama contralateral, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente).El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..
Radioterapia interna
Es una técnica de tratamiento que consiste en introducir en el interior del organismo isótopos radiactivos. Se pueden implantar de forma temporal o permanente en la zona a tratar.
Con la radioterapia interna se logra administrar altas dosis de radiación a cortas distancias, de tal forma, que llega muy poca dosis a los tejidos sanos circundantes al implante.
¿Cómo se colocan los implantes?
Dependiendo del tipo de implante que se vaya a realizar es necesario permanecer ingresado en el hospital durante 1 o dos días, en otros casos el paciente podrá irse a su casa el mismo día tras recibir el tratamiento. Bajo sedación o anestesia general, se efectuará la colocación de los isótopos radiactivos.
¿Es necesario permanecer aislado?
En ocasiones, mientras tenga colocados los implantes es necesario que permanezca en una habitación, preparada especialmente para tal fin.
El paciente estará controlado, en todo momento, a través de un monitor de televisión por el personal sanitario responsable de su cuidado.
¿Cuánto dura el tratamiento?
La duración del tratamiento dependerá en gran medida del tipo de isótopo que se haya empleado en el implante y de la cantidad de dosis que se quiera administrar en la zona del tumor, pero generalmente oscila entre minutos y días.
Cuidados de la piel
La piel es el órgano que primero recibe la radiación, por lo que es fundamental tener un cuidado especial desde el momento que se inicia el mismo.- No se aplique ningún tipo de crema, pomada o loción sobre la zona de tratamiento sin consultarlo previamente con el personal sanitario de radioterapia.
- No se cubra la zona de tratamiento con esparadrapo, tiritas, etc., ya que al tratar de despegarlos, con frecuencia se lesiona la piel.
- Lávese esa zona sólo con agua, evitando jabones. Cuando te seques, hazlo suavemente con pequeños toques.
- En general, es importante que evite lesiones como rasguños y cortes en la piel del área de tratamiento.
- No utilice desodorantes sobre la axila a radiar.
Estas recomendaciones solamente hacen referencia al área tratada; el resto del cuerpo se cuidará normalmente.
En general, es aconsejable evitar utilizar ropa ajustada. Evitar prendas con elásticos sobre la piel del tratamiento (el roce continuo podría erosionarla fácilmente).
Utiliza ropa de fibras naturales, ya que son más cómodas y menos irritantes.
Las áreas tratadas con radioterapia se vuelven muy sensibles al sol, y por lo tanto, es conveniente no exponerlas al mismo, al menos durante el primer año tras finalizar el tratamiento. Una vez pasado ese tiempo, la utilización de cremas solares, gorros, camisas de manga larga, etc., pueden ser de ayuda para reducir la exposición solar sobre la zona.
Linfedema
El linfedema se produce porque al extirpar estos ganglios linfáticos se acumula líquido intersticial en el brazo del mismo lado de la intervención, provocando un aumento de su tamaño.
El linfedema es la hinchazón del brazo de la zona que ha sufrido la intervención quirúrgica en la mama y axila. Esta hinchazón se produce por acumulación anormal de líquido intersticial debido a la interrupción de los vasos linfáticos. Como consecuencia se provoca una sobrecarga del sistema linfático, en el que el volumen de linfa acumulada excede a la capacidad de drenaje de la misma.
El linfedema es la secuela más importante del tratamiento loco-regional de cáncer de mama. Se trata de un trastorno crónico y progresivo que no todas las mujeres intervenidas de cáncer de mama desarrollan.
Se estima que una de cada cuatro mujeres desarrollará esta complicación y aunque el tiempo de aparición varía entre semanas y años, lo más frecuente es que el 75% de los casos aparezcan durante el primer año tras la cirugía.
Produce en la mayoría de los casos pesadez, episodios de infección y deformidad estética. No hay que confundirlo con un problema estético ya que se trata de un problema de salud y como tal debe abordarlo el profesional capacitado para ello, en este caso el fisioterapeuta especialista en este campo.
Las medidas preventivas para evitar la aparición del linfedema son fundamentales, ya que una vez que se establece no existe un tratamiento curativo eficaz.
La prevención del linfedema debe comenzar inmediatamente tras la cirugía y requiere una serie de cuidados diarios por tu parte, así como un seguimiento regular por parte del fisioterapeuta que será el encargado de educar a la paciente en los hábitos higiénicos sanitarios adecuados.
Inmediatamente tras la intervención el fisioterapeuta debe iniciar un programa de ejercicios respiratorios y movilidad de la mano del brazo afecto. Progresivamente, se irán introduciendo un mayor número de movimientos, que deberás llevar a cabo con suavidad y de forma repetitiva, y que pueden ser de utilidad, inmediatamente después del proceso quirúrgico, y siempre como complemento al tratamiento fisioterapéutico, ya que movilizan la cicatriz.
-
O
- Ostiosarcoma (Cáncer)
Llamamos Osteosarcoma, a aquella enfermedad tumoral procedente de las células del tejido óseo. Este tejido deriva del Mesodermo, que es la parte del embrión que va a transformarse, durante su desarrollo, en determinados tejidos como los músculos, cartílagos, articulaciones, huesos, tejidos conectivos (por ejemplo los tendones), vasos sanguíneos y linfáticos y tejidos grasos.
Los huesos están compuestos de varios tipos de tejidos: el óseo, propiamente dicho, y otros, como el colágeno, fibroso, vascular etc.. En el tejido óseo se identifican tres tipos diferentes de células: osteocitos, osteoblastos y osteoclastos. Cada una de ellas tiene una función que se complementa con la de las demás en un constante equilibrio.
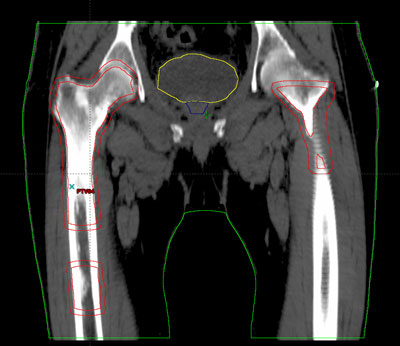
Un tumor puede aparecer en cualquier parte de un hueso. Hay una gran variedad de tumores benignos óseos, cuya característica principal es que no invaden o infiltran los tejidos de alrededor del hueso. En el hueso también pueden aparecer tumores malignos, que tienen la capacidad de invadir tejidos y dar metástasis a distancia.
El Osteosarcoma es uno de los tipos de tumores óseos que destruye el tejido óseo normal y lo debilita. Se origina en las células óseas más inmaduras que son las que generan hueso nuevo (los osteoblastos).Hay dos tipos, el medular y el periférico.
Dentro de cada uno de estos tipos hay una serie de subtipos histológicos según el aspecto de las células y su entorno al microscopio:Nombre Tejido del que derivan
Osteosarcoma Medular Osteosarcoma Periférico Convencional Yuxtacortical bien diferenciado Telangiectásico
Periostal de bajo grado Bien diferenciado Periostal de grado intermedio De células pequeñas
Superficial de alto grado El más frecuente es el osteosarcoma convencional central, suponiendo casi el 95% de todos los osteosarcomas.
Osteosarcoma e histiocitoma fibroso maligno óseo localizados
El tratamiento puede incluir los siguientes procedimientos:
- Cirugía, seguida de quimioterapia adyuvante o radioterapia. La mayoría de los pacientes también reciben quimioterapia antes de la cirugía.
- Radioterapia, cuando no se puede extirpar completamente el tumor con la cirugía.
Osteosarcoma e histiocitoma fibroso maligno óseo metastásicos
Metástasis de pulmón
Cuando el osteosarcoma o el histiocitoma fibroso maligno (HFM) se diseminan, habitualmente se diseminan hasta el pulmón. El tratamiento del osteosarcoma y el HFM con metástasis de pulmón generalmente es quimioterapia seguida de cirugía para extirpar el cáncer que se diseminó hasta el pulmón.
Metástasis ósea o hueso con metástasis de pulmón
El osteosarcoma y el histiocitoma fibroso maligno se pueden diseminar hasta el hueso o el pulmón. El tratamiento puede incluir los siguientes procedimientos:- Quimioterapia seguida de cirugía para extirpar el cáncer, seguida de quimioterapia de combinación.
- Cirugía para extirpar el tumor primario, seguida de quimioterapia y cirugía para extirpar el cáncer que se diseminó hasta otras partes del cuerpo.
Osteosarcoma e histiocitoma fibroso maligno óseo recidivantes
El tratamiento del osteosarcoma y el histiocitoma fibroso maligno óseo recidivantes puede incluir los siguientes procedimientos:- Cirugía para extirpar el tumor, con quimioterapia o sin ella.
- Samario, con trasplante de células madre o sin este, donde se usan las células madre del paciente mismo, como tratamiento paliativo para aliviar el dolor y mejorar la calidad de vida.
Cirugía
Siempre que sea posible, se puede realizar una cirugía para extirpar todo el tumor. Se puede administrar primero quimioterapia para reducir el tamaño del tumor, de modo que se pueda extraer menos tejido y hueso. Esto se llama quimioterapia neoadyuvante.
Se pueden realizar los siguientes tipos de cirugía:
- Escisión local amplia: cirugía para extirpar el tumor y parte del tejido sano alrededor del mismo.
- Cirugía para preservar el miembro: extirpación del tumor de un miembro (brazo o pierna) sin amputación, de modo de salvar la función y la apariencia del miembro. La mayoría de los pacientes de osteosarcoma en un miembro se pueden tratar con cirugía para preservar el miembro. Se extirpa el tumor mediante una escisión local amplia. Después, el tejido y hueso extirpados se pueden reemplazar con un injerto usando tejido y hueso tomado de otra parte del cuerpo del paciente, o se puede realizar un implante como el de hueso artificial. Si se encuentra una fractura en el momento del diagnóstico o durante la quimioterapia previa a la cirugía, aún puede ser posible en algunos realizar una cirugía para preservar el miembro. Si el cirujano no puede extirpar todo el tumor y suficiente tejido sano alrededor del mismo, se puede llevar a cabo una amputación.
- Amputación: cirugía para extirpar una parte de un brazo o una pierna, o todo el miembro. Esto se puede llevar a cabo si no es posible extirpar todo el tumor mediante una cirugía para preservar el miembro. Después de la amputación, se puede colocar al paciente una prótesis (miembro artificial).
- Plastía de rotación: cirugía para extirpar el tumor y la articulación de la rodilla. La parte de la pierna que queda debajo de la rodilla se une luego con la parte de la pierna que queda encima de la rodilla, con el pie mirando hacia atrás y el tobillo funcionando como una rodilla. A continuación, se puede agregar una prótesis al pie.
Hay estudios que demostraron que la supervivencia es la misma cuando la primera cirugía que se realiza es una cirugía para preservar el miembro o una amputación.
Incluso si el médico extirpa todo el cáncer que se puede observar en el momento de la cirugía, se administra quimioterapia o radioterapia a algunos pacientes después de la cirugía para destruir cualquier célula cancerosa que haya quedado. El tratamiento administrado después de la cirugía para disminuir el riesgo de que el cáncer vuelva se llama terapia adyuvante.
Quimioterapia
La quimioterapia es un tratamiento del cáncer para el que se utilizan medicamentos para detener el crecimiento de las células cancerosas, ya sea mediante su destrucción o impidiendo su multiplicación. Cuando la quimioterapia se toma por boca o se inyecta en una vena o músculo, los medicamentos ingresan en el torrente sanguíneo y pueden llegar hasta las células cancerosas de todo el cuerpo (quimioterapia sistémica). Cuando la quimioterapia se coloca directamente en la columna vertebral, un órgano o una cavidad corporal como el abdomen, los medicamentos afectan principalmente las células cancerosas de esas áreas (quimioterapia regional). La quimioterapia de combinación es el uso de más de un medicamento anticanceroso. La forma de administración de la quimioterapia depende del tipo y el estadio del cáncer que se esté tratando.
Radioterapia
La radioterapia es un tratamiento del cáncer para el que se usan rayos X de alta energía u otros tipos de radiación para destruir células cancerosas o impedir que crezcan. Hay dos tipos de radioterapia. Para la radioterapia externa se usa una máquina afuera del cuerpo que envía la radiación hacia el cáncer. Para la radioterapia interna se utiliza una sustancia radioactiva sellada en agujas, semillas, cables o catéteres, que se coloca directamente en el cáncer o cerca del mismo. La forma de administración de la radioterapia depende del tipo y del estadio del cáncer que está siendo tratado.
Las células del osteosarcoma y el HFM no se pueden destruir fácilmente mediante radioterapia. Esta se puede usar cuando queda una pequeña cantidad de cáncer después de la cirugía o se puede administrar con otros tratamientos.Tratamiento
El tratamiento de un Osteosarcoma debe de establecerse con la colaboración de los diferentes especialistas que pueden participar en él: cirujanos (traumatólogos), oncólogos médicos, etc.. Es decir, el abordaje terapéutico debe ser “multidisciplinario”, considerando las particularidades de cada paciente, desde todos lo puntos de vista.
En líneas generales se puede considerar que en los tumores de bajo grado histológico (estadios IA y IB) el tratamiento local, el quirúrgico, es el más importante. En el caso de tumores de alto grado histológico, aunque estén localizados (Estadios IIA y IIB e incluso III) la quimioterapia tiene una enorme importancia en el planteamiento terapéutico, integrándola con la cirugía. Se suele realizar inicialmente un tratamiento quimioterápico (neoadyuvante) para reducir masa tumoral, posteriormente proceder a la cirugía y finalmente completar el tratamiento con quimioterapia adyuvante.
En los estadios más avanzados el tratamiento sistémico (quimioterapia) es la base del tratamiento.
La cirugía debe de extirpar el tumor completamente, así como a las zonas de tejido normal que lo rodean. Se ha avanzado muchísimo en los últimos años en el desarrollo de técnicas quirúrgicas que permiten conservar el miembro afectado (alrededor del 70-80% de los pacientes). Sin embargo hay ocasiones en que es necesaria una amputación.
En la quimioterapia se utilizan diversos fármacos antineoplásicos en combinación, administrados en forma de ciclos. Los fármacos más utilizados son el Methotrexate, Ifosfamida, Ciclofosfamida, Adriamicina, Cisplatino y Vepesid.
En el caso de que existan metástasis pulmonares también se sabe que la resección de las mismas, cuando es posible, proporciona un beneficio importante en el control de la enfermedad y en la supervivencia.Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como la medula espinal, las glándulas parótidas, la cavidad oral, la orofaringe, la traquea, el esófago, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar. Los más empleados son una máscara de material termoplástico que se adapta al contorno del paciente.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control.- Ovario (Cáncer)
Cáncer que se forma en los tejidos del ovario (par de glándulas femeninas reproductoras en la que se forman los óvulos o huevos). La mayoría de los cánceres de los ovarios son carcinomas epiteliales de los ovarios (cáncer que empieza en las células de la superficie del ovario) o tumores malignos de células germinales del ovario (cáncer que empieza en las células de los óvulos).
Elección del tratamiento
En el tratamiento del cáncer de ovario se sigue un protocolo, es decir un conjunto de normas y pautas (plan de tratamiento) que se establecen, basándose en la experiencia científica, para el tratamiento de dicho tumor.
Estos protocolos, que se emplean de forma generalizada en todos los hospitales, recogen las indicaciones o limitaciones de tratamiento. Debido a las características especiales del cáncer de ovario, ante la sospecha de su existencia es obligado intervenir quirúrgicamente a la paciente para:- Confirmar el diagnóstico de la enfermedad.
- Conocer cual es el tipo de tumor y su extensión.
Además de servir para el diagnóstico esta intervención ya supone el tratamiento quirúrgico de la enfermedad. En función de los hallazgos de la cirugía, será necesario complementar el tratamiento con quimioterapia.Tumores de células germinales de los ovarios en estadio I
El tratamiento depende de si el tumor es disgerminoma u otro tipo de tumor de células germinales.
El tratamiento de disgerminoma puede incluir los siguientes procedimientos:- Salpingooforectomía unilateral con linfangiografía o sin esta (un estudio radiográfico del sistema linfoide, los tejidos y los órganos que filtran y destruyen sustancias dañinas y ayudan a combatir infecciones o enfermedades) o tomografía axial computarizada (serie de fotografías detalladas de áreas internas del cuerpo creadas por una computadora conectada a una máquina de rayos X).
- Salpingooforectomía unilateral seguida por observación (monitoreo cercano de la condición de una paciente pero sin administrar el tratamiento hasta que aparezcan o se modifiquen síntomas).
- Salpingooforectomía unilateral seguida por radioterapia.
- Salpingooforectomía unilateral seguida por quimioterapia.
El tratamiento de otros tumores de células germinales los siguientes procedimientos:- Salpingooforectomía unilateral seguida por observación minuciosa, o
- Salpingooforectomía unilateral seguida por quimioterapia de combinación en algunas ocasiones.
Tumores de células germinales de los ovarios en estadio II
El tratamiento depende de si el tumor es disgerminoma u otro tipo de tumor de células germinales.
El tratamiento de disgerminoma puede incluir los siguientes procedimientos:- Histerectomía abdominal total y salpingooforectomía bilateral seguida por radioterapia o quimioterapia de combinación, o
- Salpingooforectomía unilateral seguida por quimioterapia.
El tratamiento de otros tumores de células germinales puede incluir los siguientes procedimientos:- Salpingooforectomía unilateral seguida por quimioterapia de combinación.
- Cirugía de revisión (cirugía realizada después del tratamiento primario para determinar si aún quedan células tumorales).
Tumores de células germinales de los ovarios en estadio III
El tratamiento depende de si el tumor es disgerminoma u otro tipo de tumor de células germinales.
El tratamiento de disgerminoma puede incluir los siguientes procedimientos:- Histerectomía abdominal total y salpingooforectomía bilateral, con remoción del cáncer en la pelvis y en el abdomen tanto como fuera posible.
- Salpingooforectomía unilateral seguida por quimioterapia.
El tratamiento de otros tumores de células germinales puede incluir los siguientes procedimientos:- Histerectomía abdominal total y salpingooforectomía bilateral, con remoción del cáncer en la pelvis y en el abdomen tanto como fuera posible. Se administrará quimioterapia antes o después de la cirugía.
- Salpingooforectomía unilateral seguida por quimioterapia.
- Cirugía de revisión (cirugía realizada después del tratamiento primario para determinar si aún quedan células tumorales).
Tumores de células germinales de los ovarios en estadio IV
El tratamiento depende de si el tumor es disgerminoma u otro tipo de tumor de células germinales.
El tratamiento de disgerminoma puede incluir los siguientes procedimientos:- Histerectomía abdominal total y salpingooforectomía bilateral seguida por quimioterapia, con remoción del cáncer en la pelvis y en el abdomen tanto como fuera posible.
- Salpingooforectomía unilateral seguida por quimioterapia.
El tratamiento de otros tumores de células germinales puede incluir los siguientes procedimientos:- Histerectomía abdominal total y salpingooforectomía bilateral, con remoción del cáncer en la pelvis y en el abdomen tanto como fuera posible. Se administrará quimioterapia antes o después de la cirugía.
- Salpingooforectomía unilateral seguida por quimioterapia.
- Cirugía de revisión (cirugía realizada después del tratamiento primario para determinar si aún quedan células tumorales).
Opciones de tratamiento de los tumores de células germinales de los ovarios recidivantes
El tratamiento depende de si el tumor es disgerminoma u otro tipo de tumor de células germinales.
El tratamiento de disgerminoma puede incluir el siguiente procedimiento:
- Quimioterapia con radioterapia o sin esta.
El tratamiento de otros tumores de células germinales puede incluir los siguientes procedimientos:
- Quimioterapia.
- Cirugía con quimioterapia o sin esta.
Cáncer epitelial de los ovarios en estadio I y II
El tratamiento del cáncer epitelial de ovarios en estadio I y estadio II puede incluir los siguientes procedimientos:
- Histerectomía abdominal total, salpingooforectomía bilateral y omentectomía. Se extirpan los ganglios linfáticos y otros tejidos de la pelvis y el abdomen, y se examinan bajo un microscopio para identificar células cancerosas.
- Histerectomía abdominal total, salpingooforectomía unilateral y omentectomía. Se extirpan los ganglios linfáticos y otros tejidos de la pelvis y el abdomen, y se examinan bajo un microscopio para identificar células cancerosas.
Cáncer epitelial de los ovarios en estadio III y IV
El tratamiento del cáncer epitelial de los ovarios en estadio III y estadio IV puede ser cirugía para extirpar el tumor, histerectomía abdominal total, salpingooforectomía bilateral y omentectomía. Después de la cirugía, el tratamiento depende de la cantidad de tumor que quede.
Cuando el tumor que queda mide un centímetro o menos, el tratamiento suele ser quimioterapia de combinación, incluso quimioterapia intraperitoneal (IP).
Cuando el tumor que queda mide más de un centímetro, el tratamiento puede incluir los siguientes procedimientos:
- Quimioterapia de combinación, incluso quimioterapia intraperitoneal (IP).
Opciones de tratamiento para el cáncer epitelial de ovarios recidivante o persistente
El tratamiento del cáncer epitelial de ovarios recidivante puede incluir los siguientes procedimientos:- Quimioterapia con uno o más medicamentos contra el cáncer, con cirugía o sin ella.
QuimioterapiaLa quimioterapia es una de las modalidades terapéuticas más empleada en el tratamiento del cáncer. Su objetivo es destruir, empleando una gran variedad de fármacos, las células que componen el tumor con el fin de lograr la reducción o desaparición de la enfermedad.
A los fármacos utilizados en este tipo de tratamiento se les denomina fármacos antineoplásicos o quimioterápicos.
Estos fármacos llegan a prácticamente todos los tejidos del organismo y ahí es donde ejercen su acción tanto sobre las células malignas como sobre las sanas. Debido a la acción de los medicamentos sobre estas últimas, pueden aparecer una serie de síntomas más o menos intensos y generalmente transitorios, denominados efectos secundarios.
Cirugía
La cirugía es el tratamiento más común del tumor de células germinales de los ovarios. El médico puede extirpar el cáncer mediante uno de los siguientes tipos de cirugía:- Salpingooforectomía unilateral: procedimiento quirúrgico para extirpar un ovario y una trompa de Falopio.
- Histerectomía total: procedimiento quirúrgico para extirpar el útero, incluso el cuello uterino. Si el útero y el cuello uterino se extraen a través de la vagina, la operación se llama histerectomía vaginal. Si el útero y el cuello uterino se extraen al hacerse una incisión grande (corte) en el abdomen, la operación se llama histerectomía abdominal completa. Si el útero y el cuello uterino se extraen a través de una incisión pequeña (corte) en el abdomen mediante un laparoscopio, la operación se llama histerectomía laparoscópica completa.
- Salpingooforectomía bilateral: procedimiento quirúrgico para extirpar ambos ovarios y amabas trompas de Falopio.
- Citorreducción tumoral: procedimiento quirúrgico en el cual se extirpa la mayor cantidad posible del tumor. Algunos tumores no se pueden extirpar en su totalidad.
Radioterapia
La radioterapia es un tratamiento para el cáncer el cual utiliza rayos X de alta energía u otros tipos de radiación para eliminar células cancerosas. Existen dos tipos de radioterapia. La radioterapia externa utiliza una máquina fuera del cuerpo la cual envía radiación al área donde se encuentra el cáncer.
La radioterapia interna utiliza una sustancia radiactiva sellada en agujas, semillas, alambres o catéteres que se colocan directamente dentro o cerca del cáncer. La forma en que se administra la quimioterapia va a depender del tipo o estadio en que se encuentre el cáncer bajo tratamiento.
Incluso si el médico extirpa todo el cáncer visible al momento de la cirugía, algunas pacientes recibirán quimioterapia o radioterapia después de la cirugía a fin de eliminar toda célula cancerosa que pueda quedar aún.
El tratamiento administrado después de la cirugía para disminuir el riesgo de que el cáncer vuelva se llama terapia adyuvante.
Después de la radiación o la quimioterapia, en algunas ocasiones se realiza una cirugía llamada laparotomía para una segunda mirada. Esto es similar a la laparotomía que se realiza para determinar el estadio del cáncer.Durante esta segunda cirugía, el médico tomará muestras de los ganglios linfáticos y otros tejidos en el abdomen para determinar si aún queda cáncer.
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como la vejiga, el recto, las cabezas femorales.
Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona.
En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..
Radioterapia interna
Es una técnica de tratamiento que consiste en introducir en el interior del organismo isótopos radiactivos. Se pueden implantar de forma temporal o permanente en la zona a tratar.
Con la radioterapia interna se logra administrar altas dosis de radiación a cortas distancias, de tal forma, que llega muy poca dosis a los tejidos sanos circundantes al implante.¿Cómo se colocan los implantes?
Dependiendo del tipo de implante que se vaya a realizar es necesario permanecer ingresado en el hospital durante 1 o dos días, en otros casos el paciente podrá irse a su casa el mismo día tras recibir el tratamiento. Bajo sedación o anestesia general, se efectuará la colocación de los isótopos radiactivos.
¿Es necesario permanecer aislado?
En ocasiones, mientras tenga colocados los implantes es necesario que permanezca en una habitación, preparada especialmente para tal fin.
El paciente estará controlado, en todo momento, a través de un monitor de televisión por el personal sanitario responsable de su cuidado.
¿Cuánto dura el tratamiento?
La duración del tratamiento dependerá en gran medida del tipo de isótopo que se haya empleado en el implante y de la cantidad de dosis que se quiera administrar en la zona del tumor, pero generalmente oscila entre minutos y días.
-
P
- Páncreas (Cáncer)
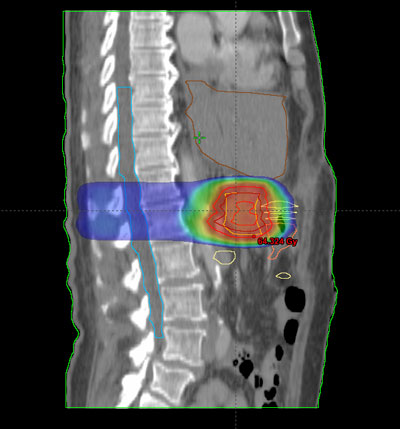
Cuando las células tumorales están ubicadas en el páncreas hablamos de cáncer de páncreas.
Cáncer de páncreas exocrino:
Las formas más habituales de cáncer de páncreas exocrino son los adenocarcinomas. Constituyen la gran mayoría de los tumores de este órgano (más del 95 %). Afectan a las células encargadas de la elaboración de los jugos digestivos y se localizan más frecuentemente en la zona de la cabeza pancreática.
Son mucho menos frecuentes los tumores del cuerpo y aún más infrecuentes los situados en la cola pancreática.
Son muy raros otros tipos de cáncer como linfomas y sarcomas.
Cáncer de páncreas endocrino:
Se consideran aparte los cánceres que afectan a las células en las que tiene lugar la síntesis de sustancias hormonales. Estos son mucho más raros (insulinomas, glucagonomas...) Poseen un curso diferente al resto de tumores pancreáticos, tanto en los síntomas como en el diagnóstico y tratamiento.
Para determinar el tratamiento más adecuado para cada caso de cáncer de páncreas, es importante clasificar el tumor y determinar en qué fase se encuentra.El sistema que con mayor frecuencia se emplea para su clasificación es el TNM. Estas siglas hacen referencia a tres aspectos del cáncer: la T se refiere al tamaño del tumor, la N a la afectación de los ganglios linfáticos y la M a la afectación o no de otros órganos.
En función de estos aspectos, la enfermedad se agrupa en las siguientes etapas o estadios:- Estadio I: el tumor afecta sólo al páncreas.
- Estadio II: el tumor afecta al duodeno o a la vesícula biliar, pero no a ganglios linfáticos.
- Estadio III: en esta etapa el tumor afecta alos ganglios linfáticos independientemente de su tamaño.
- Estadio IV: el cáncer se ha diseminado afectando a otros órganos como estómago, colon, hígado o más infrecuentemente pulmón.
Elección del tratamiento
Una vez confirmado el diagnóstico de cáncer de páncreas y tras realizar las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado.El especialista recomendará y explicará las posibilidades de tratamiento más adecuadas a su caso, para que una vez que haya recibido la suficiente información pueda, junto con su médico, tomar una decisión.
El plan de tratamiento del cáncer de páncreas es multidisciplinario y se basa en una serie de normas y pautas (protocolo), establecidas por cada hospital basándose en la experiencia clínica.
Estos protocolos, recogen las indicaciones o limitaciones de tratamiento en función de una serie de factores:- Fase en la que se encuentra la enfermedad (TNM).
- El tipo de célula que forma el tumor.
- Edad del paciente.
Probablemente, el médico también tendrá en cuenta, si además del cáncer de páncreas, existen otras enfermedades importantes que puedan dificultar la realización de algún tratamiento específico.
Por tanto el tratamiento propuesto por el especialista no va a ser el mismo en todos los pacientes.
Los tratamientos más frecuentemente empleados en el cáncer pancreático son la cirugía, la radioterapia y la quimioterapia. Independientemente de estos, el médico se encargará de tratar específicamente aquellos síntomas que presenta el enfermo.
Cáncer del páncreas en estadio I y estadio II
El tratamiento del cáncer de páncreas en el estadio I y en estadio II puede incluir los siguientes procedimientos:
- Cirugía sola.
- Cirugía con quimioterapia y radioterapia.
Cáncer del páncreas en estadio III
El tratamiento del cáncer del páncreas en el estadio III puede incluir los siguientes procedimientos:
- Cirugía paliativa o colocación de cánulas para evitar las áreas bloqueadas en los conductos o en el intestino delgado.
- Quimioterapia con gemcitabina.
Cáncer del páncreas en estadio IV
El tratamiento del cáncer del páncreas en el estadio IV puede incluir los siguientes procedimientos:
- Quimioterapia con gemcitabina, con erlotinib o sin este.
- Tratamientos paliativos para el dolor, como bloqueo de los nervios y otros cuidados médicos de apoyo.
- Cirugía paliativa o colocación de cánula para evitar las áreas bloqueadas en los conductos o en el intestino delgado.
Opciones de tratamiento para el cáncer del páncreas recidivante
El tratamiento del cáncer de páncreas recidivante puede incluir los siguientes procedimientos:
- Quimioterapia.
- Cirugía paliativa o colocación de una cánula para evitar áreas bloqueadas en conductos o en el intestino delgado.
- Radioterapia paliativa.
- Otras medidas médicas paliativas para reducir los síntomas, como el bloqueo de nervios para aliviar el dolor.
Radioterapia
La radioterapia es el empleo de radiaciones ionizantes para el tratamiento, local o locorregional, de determinados tumores que emplea rayos X con altas dosis de irradiación.
Su objetivo es destruir las células tumorales causando el menor daño posible a los tejidos sanos que rodean dicho tumor.
En el cáncer de páncreas, la radioterapia no se emplea como tratamiento exclusivo con intención curativa, ya que las dosis necesarias para destruir el tumor serían elevadas y los efectos secundarios muy serios.
Cirugía
La cirugía es el tratamiento fundamental en aquellos tumores de páncreas operables, es decir que están limitados al mismo. En ocasiones, es necesario complementarla con otros tratamientos.
La cirugía del páncreas, en cualquiera de sus modalidades, es una intervención compleja. En todos los casos es preciso que el paciente permanezca ingresado en el hospital durante un tiempo que puede variar de un enfermo a otro, pero por lo general suele durar varias semanas. Asimismo, se requiere administrar una anestesia, que siempre será de tipo general.
El tipo de cirugía que se puede aplicar en este tipo de tumor, varía en función de la localización y de la extensión de la enfermedad a ganglios y/o órganos vecinos.
Las técnicas quirúrgicas más ampliamente empleadas son:
- Pancreatoduodenectomía o cirugía de Whipple: es la técnica más empleada para tratar el cáncer de páncreas. En general consiste en la extracción de la cabeza del páncreas. Para ello es preciso extirpar el duodeno (primera porción del intestino delgado), la vesícula biliar y el conducto secretor. En este tipo de operación se deja parte del páncreas para que pueda seguir funcionando, por lo que se conecta este al intestino delgado.
- También es posible en ocasiones que la zona extirpada sea sólo la región de la cola (pancreatectomía distal).
Con este tipo de cirugía es necesario administrar insulina al paciente para controlar los niveles de azúcar en sangre.
En ocasiones, la cirugía puede emplearse como tratamiento paliativo. Si el tumor está diseminado pero provoca una obstrucción de las vías biliares, lo indicado puede ser realizar un bypass. Consiste en la colocación de un tubo que rodee la zona de obstrucción, de tal forma que los jugos pancreáticos y la bilis pasen al intestino delgado sin pasar por la zona del tumor.
Cuando por determinadas circunstancias no sea posible llevar a cabo una cirugía, se puede colocar un pequeño tubo metálico o de plástico en la zona de la obstrucción (STENT) para que se abra el conducto y permita el paso de los jugos.
Generalmente estas 2 últimas técnicas mejoran los síntomas del enfermo e incrementan su calidad de vida.Quimioterapia
En el cáncer de páncreas la quimioterapia se puede emplear en las fases iniciales de la enfermedad tras la cirugía, generalmente asociada a la radioterapia (quimioterapia adyuvante).
En ocasiones la quimioterapia se administra antes de la cirugía (quimioterapia neoadyuvante) para reducir el tamaño tumoral y facilitar así su extirpación.
Cuando la enfermedad está más avanzada o el estado del paciente no permite aplicar cirugía, el tratamiento indicado para estos casos es la administración de quimioterapia pudiéndose asociar o no a la radioterapia. En estos casos, se emplea como tratamiento paliativo y su objetivo fundamental es disminuir los síntomas derivados del tumor y mejorar la calidad de vida del paciente.
Radioterapia
La radioterapia es el empleo de radiaciones ionizantes para el tratamiento, local o locorregional, de determinados tumores que emplea rayos X con altas dosis de irradiación.
Su objetivo es destruir las células tumorales causando el menor daño posible a los tejidos sanos que rodean dicho tumor.
En el cáncer de páncreas, la radioterapia no se emplea como tratamiento exclusivo con intención curativa, ya que las dosis necesarias para destruir el tumor serían elevadas y los efectos secundarios muy serios.
La radioterapia es útil en algunos casos en los que el tumor se ha diseminado a otros órganos y pudiera estar causando algún síntoma que disminuya la calidad de vida (radioterapia paliativa). Con dosis bajas de radiación se pueden mejorar dichos síntomas y aumentar el bienestar del paciente.
Asimismo, se puede emplear asociada a la quimioterapia tras la cirugía para eliminar las células que no se han podido extirpar. En este caso la dosis de radiación tampoco debe alcanzar dosis que pudieran lesionar los órganos más sensibles próximos al tumor.Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como el estomago, el hígado, riñones, medula espinal, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..
- Próstata (Cáncer)
Cáncer que se forma en los tejidos de la próstata (una glándula del aparato reproductor masculino que se encuentra debajo de la vejiga y adelante del recto). El cáncer de próstata se presenta, por lo general, en hombres de edad avanzada.
En el 95 % de los casos, el cáncer de próstata es un adenocarcinoma. Otros tipos menos frecuentes, por los que no se trata de ellos en estos apartados son el carcinoma de células transicionales (semejante al de la vejiga), el leiomiosarcoma, fibrosarcoma o linfoma.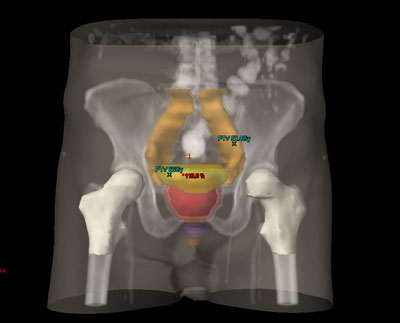
Para poder determinar el tratamiento más adecuado para el cáncer de próstata, es importante clasificar el tumor, es decir, determinar en qué fase se encuentra.
El sistema que con mayor frecuencia se emplea para su clasificación es el TNM. Estas siglas hacen referencia a 3 aspectos del cáncer: la T se refiere al tamaño del mismo, la N a la afectación de los ganglios linfáticos y la M a la afectación o no de otros órganos.
En función de estos aspectos, el cáncer de próstata se agrupa en las siguientes etapas o estadios.
- Estadio I: el cáncer no es palpable ni visible por medios diagnósticos. Su diagnóstico es accidental (cuando el paciente acude por otros motivos al urólogo).
- Estadio II: tumor palpable o visible que no sobrepasa la próstata. El tumor no se ha diseminado fuera de la próstata.
- Estadio III: el cáncer sobrepasa la cápsula y afecta a tejidos que rodean la próstata como las vesículas seminales.
- Estadio IV: El tumor se ha diseminado a los ganglios linfáticos o a otras partes del organismo, como los huesos.
La agresividad de las células tumorales se clasifica mediante un sistema denominado Gleason que determina distintas categorías de agresividad de las células. Este nombre corresponde a la del patólogo norteamericano que propuso los distintos grados.Sistema de Gleason
Este sistema valora el aspecto y distribución que las glándulas tumorales presentan al microscopio. Distingue varios tipos (grados o patrones de Gleason) clasificándolos en 5 categorías diferentes de menor a mayor agresividad. Éstas se expresan con números del uno al cinco, correspondiendo el 1 a los tumores menos agresivos y el 5 para los más agresivos.
Debido a que las células dentro del mismo cáncer de próstata no siempre son del mismo grado, actualmente se identifican los dos patrones más predominantes y se suman, obteniendo lo que se conoce como suma de Gleason o "score" de Gleason.
Este oscila entre 2 (1+1) el mínimo y 10 (5+5) el más agresivo. Hasta el grado 6 se consideran los tumores menos agresivos, del 8 hasta el 10 se incluyen los más agresivos y el tumor de grado 7 se considera intermedio.
Elección del tratamiento
Una vez que se ha confirmado el diagnóstico de cáncer de próstata y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado para curarla.
El especialista le recomendará y explicará las posibilidades de tratamiento más indicadas en su caso, para que una vez que haya recibido la suficiente información pueda, junto con su médico tomar una decisión.
El tratamiento del cáncer de próstata, como ocurre en la mayoría de los tumores, es un tratamiento multidisciplinar. Distintas especialidades trabajan juntas para combinar terapias y ofrecer al paciente las mayores posibilidades de curación.
En el tratamiento del cáncer de próstata se sigue un protocolo, es decir un conjunto de normas y pautas (plan de tratamiento) que se establecen, basándose en la experiencia científica, para el tratamiento de dicho tumor.
Estos protocolos, que se emplean de forma generalizada en todos los hospitales, recogen las indicaciones o limitaciones de tratamiento en función de una serie de factores:- Estadio de la enfermedad.
- Agresividad de las células cancerosas (suma o "score" de Gleason).
- Niveles de PSA en el momento del diagnóstico.
- Edad y esperanza de vida estadística independientemente del cáncer de próstata.
- Preferencias del paciente.
Probablemente, el médico también tendrá en cuenta si además del cáncer de próstata, existen otras enfermedades importantes, que puedan dificultar la realización de algún tratamiento específico.El tratamiento propuesto por el especialista no va a ser el mismo en todos los pacientes
Los tratamientos más frecuentemente empleados en el cáncer de próstata son la observación y vigilancia, la cirugía, la radioterapia y la hormonoterapia.
En los siguientes apartados se describen cada uno de ellos tratando de explicar en qué consisten, qué efectos adversos producen y cuáles son las recomendaciones para minimizar dichos efectos.Cáncer de próstata en estadio I
El tratamiento del cáncer de próstata en estadio I puede incluir los siguientes procedimientos:
- Espera atenta.
- Prostatectomía radical, habitualmente con linfadenectomía pélvica, con radioterapia o sin ella después de la cirugía. Puede ser posible extirpar la próstata sin dañar los nervios necesarios para la erección.
- Radioterapia de haz externo.
- Radioterapia con implante.
Cáncer de próstata en estadio II
El tratamiento del cáncer de próstata en estadio II puede incluir los siguientes procedimientos:
- Prostatectomía radical, con linfadenectomía pélvica o sin ella. Se puede administrar radioterapia después de la cirugía. Puede ser posible extirpar la próstata sin dañar los nervios necesarios para la erección.
- Espera atenta.
- Radioterapia de haz externo con terapia hormonal o sin esta.
- Radioterapia con implante.
Cáncer de próstata en estadio III
El tratamiento del cáncer de próstata en estadio III puede incluir los siguientes procedimientos:
- Radioterapia de haz externo con terapia hormonal o sin ella.
- Terapia hormonal.
- Prostatectomía radical, con linfadenectomía pélvica o sin ella. Se puede administrar radioterapia después de la cirugía.
- Espera cautelosa.
- Radioterapia, terapia hormonal o resección transuretral de la próstata como tratamiento paliativo para aliviar los síntomas causados por el cáncer.
Cáncer de próstata en estadio IV
El tratamiento del cáncer de próstata en estadio IV puede incluir los siguientes procedimientos:
- Terapia hormonal.
- Radioterapia de haz externo con terapia hormonal o sin ella.
- Radioterapia o resección transuretral de la próstata como tratamiento paliativo para aliviar los síntomas causados por el cáncer.
- Espera atenta.
Opciones de tratamiento para el cáncer de próstata recidivante
El tratamiento del cáncer de próstata recidivante puede incluir los siguientes procedimientos:
- Radioterapia.
- Prostatectomía para pacientes inicialmente tratados con radioterapia.
- Terapia hormonal.
- Medicamentos para el dolor, radioterapia externa, radioterapia interna con radioisótopos como estroncio-89, u otros tratamientos como terapia paliativa para reducir el dolor de hueso.
Cirugía
El tipo de cirugía que se puede aplicar en el cáncer de próstata, varía en función del tamaño, de la localización y de la extensión de la enfermedad a ganglios y/o órganos vecinos.
La cirugía a nivel de la próstata es una intervención quirúrgica mayor, por lo que es necesario un ingreso hospitalario durante un tiempo que puede variar de un enfermo a otro, pero por lo general suele oscilar entre una y dos semanas. Asimismo, es necesario una anestesia, que siempre será de tipo general.
Se lleva a cabo mediante una intervención denominada prostatectomía radical. Se realiza como tratamiento definitivo y su objetivo es conseguir la curación del cáncer.
Generalmente, su indicación es, exclusivamente, para aquellos pacientes con enfermedad limitada a la glándula prostática.
Consiste en la extirpación de la glándula prostática por completo. Además, se extirpan también las vesículas seminales con las que se encuentra íntimamente relacionada, y en determinadas ocasiones, se hará una extirpación de los ganglios linfáticos regionales que sirven de drenaje a la próstata.Una vez completada la extirpación, la vejiga de la orina y la uretra quedan desconectadas, ya que también se extirpa la porción de uretra que atraviesa la próstata. A continuación, el cirujano procederá a unir estas estructuras mediante puntos de sutura, colocando además una sonda urinaria que deberá llevar durante unos días.
Tras la intervención, siempre y cuando todo discurra sin complicaciones, permanecerá hospitalizado durante unos días, generalmente una semana, al cabo de los cuales será dado de alta. Lo habitual es que se vaya a su casa con la sonda urinaria y los puntos de sutura de la herida quirúrgica.
Después de una prostatectomía radical desaparecerá la emisión de semen debido a que las estructuras extirpadas son las que lo producen, prácticamente, en su totalidad.
Actualmente, las técnicas quirúrgicas para practicar una prostatectomía radical son:- PROSTATECTOMÍA RADICAL RETROPÚBICA: se llega a la próstata a través del abdomen, realizando una incisión desde el ombligo hasta el pubis. Tras la intervención quedará una cicatriz en dicha zona. Su práctica es la más extendida actualmente.
- PROSTATECTOMÍA RADICAL PERINEAL: en este caso la extirpación de la próstata se hace mediante una incisión practicada en el periné (área existente entre el ano y la bolsa escrotal que alberga los testículos).
- PROSTATECTOMÍA RADICAL LAPAROSCÓPICA: consiste en practicar varias punciones en la cavidad abdominal que permiten colocar unos tubos (trocares) a través de los cuales el cirujano opera mirando las imágenes recogidas por una cámara en un monitor de televisión. Esta técnica permite extraer la próstata y vesículas seminales sin dejar herida quirúrgica. Tan sólo quedan unas pequeñas cicatrices correspondientes a las incisiones realizadas para situar los trocares.
Quimioterapia
La quimioterapia en el cáncer de próstata avanzado se indica en pacientes que no responden o hayan dejado de responder al tratamiento hormonal.
Tratamiento hormonal
Desde hace años se sabe que el cáncer de próstata es un tumor, en la mayoría de los casos, dependiente de las hormonas y, particularmente, de los andrógenos.
Estos son producidos en su mayor parte (90-95%) en los testículos en forma de testosterona y el resto (5-10%) en las glándulas suprarrenales, que se encuentran situadas encima de ambos riñones. Los andrógenos actúan sobre la próstata estimulando la proliferación de las células tumorales.
Los tratamientos hormonales se utilizan sobre todo cuando la enfermedad está diseminada o bien como complemento de alguno de los tratamientos locales o en las recaídas que pueden presentarse tras dichos tratamientos.
La eficacia del tratamiento hormonal se basa en suprimir la testosterona de la sangre, y por tanto el efecto que esta tiene sobre el cáncer de próstata, lo que ocurre en el 80% de los casos.
La supresión de los andrógenos se va a conseguir mediante tratamiento farmacológico (medicamentos) o mediante tratamiento quirúrgico, extirpando los testículos o su tejido productor de testosterona (orquidectomía).
- Orquidectomía: generalmente se efectúa una extirpación de la parte interior del testículo donde está el tejido productor de testosterona. Es una intervención sencilla que requiere anestesia y una breve hospitalización que, generalmente, no supera 24 horas. Los efectos hormonales derivados de la orquidectomía son inmediatos produciéndose un descenso eficaz sobre el cáncer de próstata en menos de 24 horas.
Este tratamiento no es reversible y genera una deprivación de testosterona definitiva.
- Tratamiento farmacológico: consiste en obtener la supresión de la testosterona mediante medicamentos (análogos de la LHRH) que actúan sobre la hipófisis consiguiendo que los testículos dejen de producir esta hormona. Esto se logra mediante unas inyecciones que permiten que el efecto dure hasta tres meses, con la consiguiente comodidad, ya que sólo serán necesarias cuatro inyecciones al año. Para evitar la acción de los andrógenos procedentes de la glándula suprarrenal se utilizan los antiandrógenos. En ocasiones, se usan conjuntamente con los análogos de la LHRH conociéndose esta modalidad de tratamiento como bloqueo hormonal completo.
El tratamiento con medicamentos tiene la ventaja de ser reversible, de manera que si aparecen efectos secundarios, se puede suspender volviendo a una situación hormonal igual a la existente antes del tratamiento. Los inconvenientes son que tiene que preocuparse de tomar la medicación con la periodicidad prescrita por el especialista, y que tardan unas semanas en alcanzar su eficacia. Con el tiempo, el tratamiento hormonal puede fracasar al proliferar células que presentan la característica de ser resistentes a las hormonas, produciéndose entonces la progresión de la enfermedad, situación que se conoce como hormonoresistencia.
Efectos secundarios
Tras la deprivación de andrógenos en la sangre aparecen ciertos efectos secundarios que pueden disminuir la calidad de vida. Entre los más importantes destacan la aparición de impotencia, disminución de la líbido (deseo sexual), aumento de peso, desarrollo discreto de las mamas, debilidad muscular, anemia, osteoporosis y sofocos.(deseo sexual), aumento de peso, desarrollo discreto de las mamas, debilidad muscular, anemia, osteoporosis y sofocos.
¿Es necesario permanecer aislado?
En ocasiones, mientras tenga colocados los implantes es necesario que permanezca en una habitación, preparada especialmente para tal fin.
El paciente estará controlado, en todo momento, a través de un monitor de televisión por el personal sanitario responsable de su cuidado.
¿Cuánto dura el tratamiento?
La duración del tratamiento dependerá en gran medida del tipo de isótopo que se haya empleado en el implante y de la cantidad de dosis que se quiera administrar en la zona del tumor, pero generalmente oscila entre minutos y días.Radioterapia
La radioterapia es el empleo de radiaciones ionizantes para el tratamiento, local o locorregional, de determinados tumores que emplea rayos X con altas dosis de irradiación.
Las radiaciones ionizantes poseen la capacidad de destruir las células tumorales en la zona donde son aplicadas. Desde hace tiempo se conoce la sensibilidad del cáncer de próstata a determinadas radiaciones, por lo cual la radioterapia constituye un tratamiento muy eficaz para esta enfermedad.
Es un tratamiento local cuyo objetivo es, al igual que la cirugía, conseguir la curación del cáncer. Generalmente, como tratamiento exclusivo está indicado en pacientes con tumores localizados en la próstata. Cuando el tumor está localmente avanzado (tumores que sobrepasan los límites de la próstata) se consigue, en ocasiones, el control tumoral y la mejoría de la calidad de vida.
Existen dos modalidades de aplicación de la radioterapia:
- Radioterapia externa: consiste en la administración de las radiaciones desde el exterior mediante unos equipos generadores de radiación (aceleradores lineales), que no contactan con el paciente y emiten y proyectan estas sobre la próstata.
- Braquiterapia: la radiación se administra mediante fuentes de material radiactivo colocadas en estrecho contacto con la próstata.
Existen dos tipos de braquiterapia en la próstata: implantes permanentes y temporales.
El tratamiento con radioterapia siempre es individualizado, es decir, cada enfermo tendrá su tratamiento específico y distinto al de otro paciente.
Según la finalidad con que se emplee, la radioterapia puede ser curativa o paliativa para aliviar síntomas provocados por el cáncer de próstata tales como el dolor óseo.
En los últimos años los avances de la tecnología han permitido mejorar la eficacia de este tratamiento disminuyendo, notablemente, sus efectos secundarios. Con los modernos equipos de radioterapia (conformacional en tres dimensiones y de intensidad modulada) se calcula y administra al tumor la dosis de radiación con gran precisión, minimizando la dosis que reciben los tejidos sanos de alrededor de la próstata.
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como la vejiga, el recto, las cabezas femorales, el bulbo peneano, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..
Radioterapia interna
Es una técnica de tratamiento que consiste en introducir en el interior del organismo isótopos radiactivos. Se pueden implantar de forma temporal o permanente en la zona a tratar.
Con la radioterapia interna se logra administrar altas dosis de radiación a cortas distancias, de tal forma, que llega muy poca dosis a los tejidos sanos circundantes al implante.
¿Cómo se colocan los implantes?
Dependiendo del tipo de implante que se vaya a realizar es necesario permanecer ingresado en el hospital durante 1 o dos días, en otros casos el paciente podrá irse a su casa el mismo día tras recibir el tratamiento. Bajo sedación o anestesia general, se efectuará la colocación de los isótopos radiactivos.Incontinensia Urinaria
La pérdida involuntaria de la orina puede aparecer tras el tratamiento. Se produce como consecuencia de la proximidad de la próstata al esfínter urinario, el cual durante el procedimiento terapéutico puede verse lesionado, así como algunas de las estructuras involucradas en la continencia.
Esta situación produce un insuficiente funcionamiento de los mecanismos responsables en la retención urinaria y, por consiguiente, la aparición de incontinencia. La edad es un factor de riesgo, de modo que los enfermos de más edad son los que con mayor frecuencia presentan incontinencia postoperatoria.
La pérdida de orina puede ser diferente según los casos, distinguiéndose tres tipos:
- Urgencia miccional: en esta circunstancia la vejiga se contrae sin haber voluntad de hacerlo, provocando un intenso deseo de orinar que obliga a la micción.
- Incontinencia de esfuerzo: los escapes de orina ocurren cuando se realizan movimientos o ejercicios que aumentan la presión en el abdomen como puede ser al moverse súbitamente, correr, levantarse de una silla, etc.
- Incontinencia total: es la pérdida constante y continua de orina no llegando a realizar micciones, o pocas, debido a que no se llega a almacenar prácticamente orina en la vejiga.
Las primeras medidas que se pueden adoptar para mejorar esta situación son la restricción de líquidos y realización de ejercicios que están destinados a fortalecer los músculos del suelo de la pelvis, ayudando a disminuir la incontinencia.
Si las pérdidas son cuantiosas y ha transcurrido el tiempo suficiente como para considerar que es una incontinencia establecida, se pueden plantear tratamientos para mejorar o resolver esta.
Tratamiento de la incontinencia
Este tratamiento consiste en intervenciones quirúrgicas que llevan a cabo la inyección de substancias como colágena o silicona a través de la uretra en las proximidades del esfínter, produciendo el cierre parcial de éste.
Otra solución más compleja, es la colocación de un esfínter artificial mediante un manguito alrededor de la uretra, que al llenarse de líquido cierra la uretra.
Dispositivos para la incontinencia urinaria
La incontinencia puede variar en su intensidad requiriendo desde el uso de una pequeña gasa de protección, pasando por el empleo de compresas hasta llegar a la necesidad de tener que llevar pañal, con la consiguiente incomodidad y afectación psicológica y social.
Actualmente, existen en el mercado una importante variedad de dispositivos adaptados a las distintas necesidades de cada paciente que permiten, de forma discreta y eficaz, paliar las incomodidades y alteraciones de la pérdida de orina proporcionando la posibilidad de seguir llevando una vida normal.
- Absorbente masculino: su uso está indicado, principalmente, en aquellos pacientes con incontinencia de goteo. Se trata de una compresa fina y absorbente en forma de bolsa con una gran capacidad de absorción. Este material asegura la retención de toda la humedad sin posibilidad de fuga.
- Cooreslect: Se trata de un sistema fabricado con un material sintético sin látex e hipoalergénico, que se adapta al pene como un preservativo, quedando sujeto a él por una tira autoadhesiva, que evita que se mueva y exista pérdida de orina.
Existen varias modalidades y tamaños para adaptarse a las distintas necesidades de los pacientes.
El colector drena hacia una bolsa de recogida de orina, que mediante unas cintas se fija a la pierna (como si se tratara de un liguero). Es un sistema cómodo y discreto que permite desarrollar la actividad diaria normalmente.Disfunción sexual
Es la alteración en la capacidad de erección o de su duración, impidiendo o dificultando la actividad sexual. Es una circunstancia que ocurre con cierta frecuencia tras los tratamientos del cáncer de próstata.
En los primeros momentos después de conocer el diagnóstico, este aspecto puede pasar a un segundo plano dando prioridad a la curación de la enfermedad. Después del tratamiento, con el paso del tiempo llega a ser una preocupación importante que produce un grado de insatisfacción considerable que altera la calidad de vida. Esto se hace más evidente cuanto más joven es el paciente.
Es muy frecuente que tras los tratamientos se produzca una falta de emisión de semen con el orgasmo, esta situación se conoce como orgasmo seco. La satisfacción de la actividad sexual no tiene por qué verse afectada.
La disfunción sexual se produce como consecuencia de la lesión o extirpación de los nervios y vasos sanguíneos responsables de la erección en el tratamiento quirúrgico o la radioterapia. Si no se preservan, la práctica totalidad permanecen impotentes. Hay que tener presente que la preservación de los nervios de la erección no se puede hacer en todos los pacientes sometidos a prostatectomía radical.
Influyen claramente, la edad y la función sexual previa al tratamiento. Cuanto mayor es la edad en el momento del tratamiento mayores probabilidades hay de perder la función sexual después del mismo. En el caso de tener la potencia sexual alterada antes de la cirugía o radioterapia, esta se va a ver afectada con mayor frecuencia.
En el caso de la cirugía, la pérdida de la función sexual prácticamente es inmediata recuperándose lentamente incluso hasta dos años después de la misma. La frecuencia con la que esta capacidad de erección se mantiene o recupera varía con la técnica empleada (entre un 40 y 60% cuando se preservan indemnes los nervios), siendo mayor este porcentaje cuanto menor es la edad del enfermo.
En el caso de la radioterapia, la pérdida de la potencia sexual se produce poco a poco después del tratamiento, a medida que las radiaciones hacen su efecto sobre los tejidos.
Existen diversos tratamientos mediante los cuales se puede mejorar la potencia sexual consiguiendo una erección que permita desarrollar una actividad sexual para el enfermo y su pareja.
- Tratamiento farmacológico: mediante la utilización de medicamentos en forma de pastillas que facilitan las respuestas naturales al estímulo sexual a nivel del pene. Estos tratamientos no son eficaces en todos los enfermos sometidos a tratamiento por cáncer de próstata pero, en muchos de ellos, ayudan a mejorar este aspecto recuperando la calidad de vida alterada por esta circunstancia.
- Dispositivos de vacío: son unos mecanismos mediante los cuales se consigue el relleno del pene con la sangre por succión, alcanzando una turgencia considerable del mismo. Esta se mantiene con la colocación de un anillo constrictor en la base del pene.
Tratamiento quirúrgico: son las prótesis de pene. Existen diversos modelos en el mercado con las cuales se consigue una erección implantando unos cilindros en el interior del pene, que permiten obtener una turgencia adecuada para poder mantener una actividad sexual satisfactoria. La colocación requiere una operación que puede presentar complicaciones por la propia intervención o por el fallo en el funcionamiento de alguno de los mecanismos de la prótesis.- Pulmon (Cáncer)
Cáncer que se forma en los tejidos del pulmón, por lo general, en las células que recubren las vías respiratorias. Los dos tipos más importantes de cáncer de pulmón son el cáncer de pulmón de células pequeñas y el cáncer de pulmón de células no pequeñas. Estos tipos de cáncer se diagnostican con base en el aspecto que tengan las células bajo un microscopio.
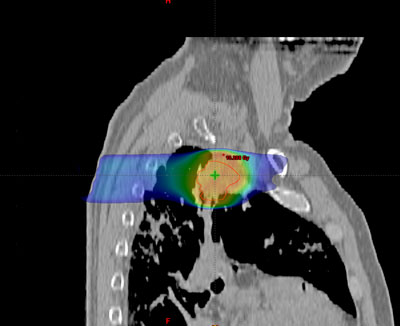
Los distintos tipos histológicos tienen diferente evolución natural y, por tanto, como paso previo al tratamiento, es necesario un diagnóstico histológico preciso realizado por un anatomopatólogo experto. Las principales decisiones con respecto al tratamiento se toman al distinguir claramente un carcinoma de célula pequeña y los que no corresponden a este tipo (subclasificados a su vez en diferentes tipos histológicos).
Las formas más comunes de cáncer de pulmón reciben nombres que dependen de las características de las células de las cuales derivan, distinguiéndose dos grandes grupos:
Carcinomas de células pequeñas o microcítico: su nombre deriva del tamaño de sus células (microcítico: células muy pequeñas). Un 20% de los cánceres de pulmón son de este tipo. Se localiza preferentemente en la zona central de los pulmones, pudiendo comprimir a vasos u órganos localizados en ese nivel (vena cava, etc.). Se caracterizan por su alta agresividad y crecimiento rápido.
Carcinomas no microcíticos: representan el 80% restante de los cánceres de pulmón. Los tipos más frecuentes son:
- Carcinoma escamoso o epidermoide: es la variedad de cáncer broncopulmonar más frecuente en nuestro país, representando el 40% de los carcinomas no microciticos. Suele localizarse en la parte central de los pulmones, y con frecuencia se necrosa en su interior y se asemeja a un absceso. Tiene un crecimiento relativamente lento.
- Adenocarcinoma: representa el 30% de los carcinomas no microcíticos. Es el menos relacionado con el consumo de tabaco, pero aún así es más frecuente en fumadores. Suele aparecer más entre las mujeres y localizarse en zonas más periféricas de los pulmones, por lo que frecuentemente afectan a la pleura y pared torácica. En los últimos años, esta variante histológica ha cobrado especial interés al descubrirse que un subgrupo de pacientes tienen una alteración molecular (mutación del EGFR) que permite ser tratados con fármacos de diana terapéutica.
Carcinoma de células grandes: se denomina así por el tamaño de las células que lo componen. Es el tipo menos frecuente de los carcinomas broncopulmonares, representando el 10% de ellos.
- Para poder emitir un juicio sobre el pronóstico del enfermo y determinar el tratamiento más adecuado, es importante clasificar el tumor, es decir, determinar en qué fase se encuentra.
El sistema que con mayor frecuencia se emplea para su clasificación es el TNM. Estas siglas hacen referencia a tres aspectos del cáncer: la T se refiere al tamaño y localización del tumor, la N a la afectación de los ganglios linfáticos y la M a la afectación o no de otros órganos.Tumor primario (T):
- T0 - No hay signos de un tumor primario.
- TX - Cáncer oculto, demostrado en la citología del lavado bronquial pero no radiológicamente ni en la fibrobroncoscopia. Las secreciones broncopulmonares contienen células malignas pero no hay otros datos de la existencia de un cáncer de pulmón.
- TIS - Carcinoma in situ.
- T1 - Tumor menor o igual de 3 cm de dimensión máxima, rodeado por tejido pulmonar o pleural visceral y sin invasión proximal al bronquio lobar en la fibrobroncoscopia.
- T2 - Tumor mayor de 3 centímetros de dimensión mayor o tumor de cualquier tamaño que invade la pleura visceral o con atelectasia (colapso del pulmón) o neumonitis obstructiva que se extiende a la región hiliar. En la broncoscopia, la extensión proximal del tumor puede limitarse al bronquio lobar o estar al menos a 2 cm de la carina. La atelectasia o la neumonitis obstructiva no deben afectar a todo un pulmón.
- T3 - Tumor de cualquier tamaño con extensión directa a la pared costal (incluidos los tumores de la cisura superior) diafragma, pleura mediastínica o pericardio, sin afectación del corazón, grandes vasos, tráquea, esófago, cuerpos vertebrales o un tumor del bronquio principal a menos de 2 cm de la carina, sin infiltración de la misma. La atelectasia afecta a todo un pulmón. Existe derrame pleural no maligno.
- T4 - Tumor de cualquier tamaño con infiltración del mediastino o del corazón, grandes vasos, tráquea, esófago, cuerpos vertebrales o carina o con derrame pleural maligno. Los derrames pleurales no hemáticos ni exudativos y con varios estudios citológicos negativos no se clasifican como malignos con fines de determinación del estadio.
Ganglios linfáticos regionales (N):- N0 - Sin metástasis demostrables en los ganglios linfáticos
- N1 - Metástasis en los ganglios linfáticos peribronquiales o hiliares ipsolaterales, o ambos, incluyendo la extensión directa del tumor.
- N2 - Metástasis en los ganglios mediastínicos o subcarinales ipsilaterales.
- N3 - Metástasis en los ganglios mediastínicos o hiliares contralaterales, escaleno ipso o contralateral o supraclaviculares.
Metástasis a distancia (M):- M0 - Sin metástasis a distancia conocidas.
- M1 - Metástasis a distancia presentes, especificando su localización por ejemplo en cerebro.
Elección del tratamiento
Una vez que se ha confirmado el diagnóstico de cáncer de pulmón, y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado para curarla. El especialista recomendará y explicará las posibilidades de tratamiento más óptimas en cada caso, para que el paciente con toda la información pueda junto con el médico tomar una decisión.
El tratamiento del cáncer de pulmón, como ocurre en la mayoría de los tumores, es multidisciplinar. Distintas especialidades trabajan juntas para combinar terapias y ofrecer al paciente las mayores posibilidades de curación. Fundamentalmente colaboran neumólogos, radiólogos, anatomopatólogos, cirujanos y oncólogos.
En el tratamiento del cáncer de pulmón se sigue un protocolo, es decir un conjunto de normas y pautas (plan de tratamiento), establecidas en base a la experiencia científica que se tiene en el tratamiento de este tumor.
Estos protocolos, que se emplean de forma generalizada en todos los hospitales, recogen las indicaciones o limitaciones del tratamiento en función de los siguientes factores:
- Fase o estadio en la que se encuentra la enfermedad (TNM).
- Tipo de tumor: carcinomas microcíticos y no microcíticos.
Características del paciente: edad, enfermedades que dificulten algún tratamiento específico, estado nutricional…
- El tratamiento propuesto por el especialista no va a ser el mismo en todos los pacientes.
Los tratamientos más frecuentemente empleados en el cáncer de pulmón son la cirugía, la radioterapia y la quimioterapia. Además el médico se encargará de tratar específicamente los síntomas que presenta cada enfermo.Cáncer de pulmón de células pequeñas
Cáncer de pulmón de células pequeñas en estadio limitado
El tratamiento del cáncer de pulmón de células pequeñas en estadio limitado puede incluir los siguientes procedimientos:- Quimioterapia de combinación y radioterapia dirigida al pecho. Más tarde, se puede administrar radioterapia dirigida al cerebro para pacientes con respuestas completas.
- Quimioterapia de combinación para pacientes con problemas pulmonares que están muy enfermos. Más tarde, se puede administrar radioterapia dirigida al cerebro para pacientes con respuestas completas.
- Cirugía, seguida por quimioterapia o quimioterapia más radioterapia dirigida al pecho. Más tarde, se puede administrar radioterapia dirigida al cerebro para pacientes con respuestas completas.
Cáncer de pulmón de células pequeñas en estadio extensivo
El tratamiento del cáncer de pulmón de células pequeñas en estadio extensivo puede incluir los siguientes procedimientos:
- Quimioterapia de combinación. Más tarde, se puede administrar radioterapia dirigida al cerebro para pacientes con respuestas completas.
- Radioterapia dirigida al cerebro, la médula, los huesos u otras partes del cuerpo en las cuales se ha diseminado el cáncer, como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
Opciones de tratamiento para el cáncer de pulmón de células pequeñas recidivante
El tratamiento del cáncer recidivante de pulmón de células pequeñas puede incluir los siguientes procedimientos:
- Quimioterapia.
- Radioterapia, como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
- Terapia láser, colocación de una derivación para mantener abiertas las vías respiratorias o radioterapia interna como tratamiento paliativo para aliviar los síntomas y mejorar la calidad de vida.
Cáncer de pulmón de células no pequeñas
Cáncer de pulmón de células no pequeñas oculto
El tratamiento del cáncer de pulmón de células no pequeñas oculto depende del sitio hasta donde el cáncer se diseminó. Por lo general, se puede curar mediante cirugía.
Estadio 0 (carcinoma in situ)
El tratamiento del estadio 0 puede incluir los siguientes procedimientos:
- Cirugía (resección en cuña o resección segmentaria).
- Terapia fotodinámica con el uso de un endoscopio.
- Electrocauterización, criocirugía o cirugía láser con el uso de un endoscopio.
Cáncer de pulmón de células no pequeñas en estadio I
El tratamiento del cáncer de pulmón de células no pequeñas en estadio I puede incluir los siguientes procedimientos:
- Cirugía (resección en cuña, resección segmentaria, resección en manguito o lobectomía).
- Radioterapia externa (para pacientes que no pueden o eligen no someterse a cirugía).
Cáncer de pulmón de células no pequeñas en estadio II
El tratamiento del cáncer de pulmón de células no pequeñas en estadio II puede incluir los siguientes procedimientos:
- Cirugía (resección en cuña, resección segmentaria, resección en manguito o lobectomía, o neumonectomía).
- Radioterapia externa (para pacientes que no pueden o eligen no someterse a cirugía).
- Cirugía seguida de quimioterapia.
Cáncer de pulmón de células no pequeñas en estadio IIIA
El tratamiento del cáncer de pulmón de células no pequeñas en estadio IIIA que se puede extirpar por medio de cirugía puede incluir los siguientes procedimientos:
- Cirugía seguida de quimioterapia.
El tratamiento del cáncer de pulmón de células no pequeñas en estadio IIIA
que no se puede extirpar por medio de cirugía puede incluir los siguientes procedimientos:
- Quimioterapia combinada con radioterapia.
- Radioterapia externa sola (para pacientes que no se pueden tratar con terapia combinada).
El cáncer de pulmón de células no pequeñas del surco superior, que a menudo se llama tumor de Pancoast, empieza en la parte superior del pulmón y se disemina hasta los tejidos cercanos como las costillas y las vértebras. El tratamiento de los tumores de Pancoast puede incluir los siguientes procedimientos:
- Radioterapia sola.
- Radioterapia y cirugía.
- Cirugía sola.
- Quimioterapia combinada con radioterapia y cirugía.
Algunos tumores de pulmón de células no pequeñas en estadio IIIA que crecieron en la pared torácica se pueden extirpar completamente. El tratamiento de los tumores de la pared torácica puede incluir los siguientes procedimientos:
- Cirugía.
- Cirugía y radioterapia.
- Radioterapia sola.
- Quimioterapia combinada con radioterapia o cirugía.
Cáncer de pulmón de células no pequeñas en estadio IIIB
El tratamiento del cáncer de pulmón de células no pequeñas en estadio IIIB puede incluir los siguientes procedimientos:
- Quimioterapia combinada con radioterapia externa.
- Radioterapia externa como terapia paliativa para aliviar el dolor y otros síntomas, y mejorar la calidad de vida.
Cáncer de pulmón de células no pequeñas en estadio IV
El tratamiento del cáncer de pulmón de células no pequeñas en estadio IV puede incluir los siguientes procedimientos:
- Radioterapia externa, como terapia paliativa para aliviar el dolor y otros síntomas, y mejorar la calidad de vida.
- Quimioterapia de combinación.
- Quimioterapia de combinación y terapia dirigida.
- Terapia láser o radioterapia interna con el uso de un endoscopio.
Opciones de tratamiento para el cáncer de pulmón de células no pequeñas recidivante
El tratamiento del cáncer de pulmón de células no pequeñas recidivante puede incluir los siguientes procedimientos:
- Radioterapia externa, como terapia paliativa para aliviar el dolor y otros síntomas, y mejorar la calidad de vida.
- Quimioterapia o terapia dirigida.
- Cirugía (para algunos pacientes que tienen una cantidad muy baja de cáncer que se diseminó hasta el cerebro).
- Terapia láser o radioterapia interna con el uso de un endoscopio.
- Radiocirugía (para ciertos pacientes que no pueden someterse a cirugía).
Cirugía
La cirugía es la primera opción de tratamiento, la más eficaz, en los cánceres no microcíticos en estadios localizados. En los carcinomas microcíticos, la primera opción de tratamiento es la quimioterapia.
El tipo de cirugía dependerá del tamaño, localización y extensión del tumor. Cuando se extirpa un lóbulo pulmonar (cada una de las partes en las que está dividido el pulmón) se llama lobectomía, cuando lo que se extirpa es todo un pulmón hablamos de neumonectomía.
La cirugía a nivel del pulmón es una intervención mayor, por lo que es necesario un ingreso hospitalario que puede variar de un enfermo a otro, pero que por lo general suele oscilar entre una y dos semanas.Asimismo, precisa anestesia, que siempre será de tipo general.
Para llevar a cabo la intervención se debe realizar una toracotomía, es decir una incisión en el tórax, que permita al cirujano llegar hasta la zona tumoral. Si solamente está afectado un lóbulo se hace una lobectomía.
Si están afectados más de un lóbulo o el bronquio principal, la intervención necesaria es la neumonectomía. Normalmente se extirpan los ganglios mediastínicos para ver si están o no afectados por el tumor.Quimioterapia
Tratamiento adyuvante (tras la cirugía)
Los pacientes con carcinoma de pulmón no microcítico sometidos a una resección completa, presentan, sin embargo, un elevado riesgo de recidiva (50% en el estadio IB, 70% en el II y un porcentaje todavía mayor de los pacientes con tumores en estadio IIIB). Es por ello que el uso de quimioterapia adyuvante (tras la cirugía) se ha estudiado desde hace varias décadas. Los primeros estudios, que se realizaron en los años 70 y 80 del siglo XX, identificaron a los derivados del platino como agentes activos para el tratamiento de este tipo de cáncer.
En los últimos años se han realizado varios ensayos clínicos para explorar la efectividad y forma de administración óptima de los regímenes de poliquimioterapia (basados en combinaciones con sales de platino). Los estudios más importantes publicados recientemente (IALT, BIG, ALPI, ANITA y JBR10), exploraban diferentes combinaciones de cisplatino (principalmente con vinorelbina) y encontraron un beneficio en cuanto supervivencia global y supervivencia libre de progresión.
Es por ello que se ofrece la posibilidad de recibir quimioterapia adyuvante en aquellos pacientes operados de cáncer de pulmón en estadio II ó III.
Tratamiento de la enfermedad localmente avanzada
El tratamiento del carcinoma no microcítico de pulmón localmente avanzado es un campo de investigación activa en el momento actual.
Generalmente, los pacientes en estadio IIIA según la clasificación de estadificación anatomopatológica suelen ser sometidos a cirugía y posteriormente tratados con quimioterapia adyuvante.
A los pacientes con derrame tumoral pleural o pericárdico suele ofrecérseles quimioterapia paliativa ya que, a pesar de que actualmente se clasifica estos casos como IIIB, el pronóstico y la evolución de estos pacientes es similar al de aquellos con enfermedad extratorácica.
De hecho, en la revisión propuesta de la clasificación TNM, estos tumores se consideran estadio IV.
Para el resto de pacientes con tumores en estadio III, el tratamiento varía entre la administración de quimio y radioterapia neoadyuvantes, seguida de resección quirúrgica y un número variable de ciclos de quimioterapia de consolidación, ó la utilización de quimiorradioterapia concomitante (esto es, darlos conjuntamente).
Tratamiento de la enfermedad avanzada
El valor del tratamiento quimioterápico para los pacientes con carcinoma no microcítico de pulmón metastásico se puso de manifiesto a raíz de los estudios en los que se comparaba el tratamiento con quimioterapia basada en cisplatino y tratamiento de soporte frente al tratamiento de soporte sin quimioterapia.
Se observó una diferencia estadísticamente significativa en supervivencia global a favor del tratamiento quimioterápico.
Existen múltiples agentes activos en el tratamiento del CPNCP, que se han utilizado tanto en combinación como en monoterapia.
Los más utilizados son los derivados de platico (cisplatino y carboplatino), los taxanos (paclitaxel y docetaxel), vinorelbina, gemcitabina, etopósido y permetrexed.
En los últimos años se han producido avances muy significativos en el tratamiento del cáncer de pulmón, incorporando nuevos fármacos dirigidos a dianas específicas de las células tumorales. Es el caso de los fármacos dirigidos al EGFR ( receptor del factor de crecimiento epidérmico) o al VEGF (factor de crecimiento derivado del endotelio vascular)Otros tratamientos
Láser intrabronquial
Cuando el desarrollo del tumor es intrabronquial, es decir dentro del conducto del bronquio, puede obstaculizar el paso del aire dificultando gravemente la respiración.En estos casos puede tratarse la lesión con láser, para destruir parte del tumor, permitir el paso del aire, y disminuir así el ahogo del paciente. El láser se aplica con la ayuda de un endoscopio introducido en las vías respiratorias.
Prótesis endobronquiales
Esta técnica, como la anterior, se utiliza cuando el desarrollo del tumor ocupa el interior de los bronquios impidiendo el paso del aire.Consiste en colocar mediante endoscopia una especie de tubo más o menos rígido a la altura de la zona del bronquio obstruida por el tumor, con el objetivo de facilitar la respiración del paciente.
Radiofrecuencia
En los últimos años han aparecido técnicas de ablación con catéteres de lesiones únicas pulmonares en pacientes inoperables.Esta técnica consiste en quemar la lesión mediante un catéter que se introduce en el pulmón. Suele usarse en tumores menores de 4 cm y todavía no es una técnica estándar de tratamiento.
Radioterapia
La radioterapia es el empleo de radiaciones ionizantes para el tratamiento, local o locorregional, de determinados tumores que emplea rayos X con altas dosis de irradiación.
Su objetivo es destruir las células tumorales causando el menor daño posible a los tejidos sanos que rodean dicho tumor. El tipo de radioterapia utilizada en el cáncer de pulmón es la externa. Para ello se emplean máquinas de gran tamaño (aceleradores lineales), que en ningún momento contactan con el enfermo.
La radioterapia puede emplearse como tratamiento único o en combinación. Se puede administrar antes de la intervención para disminuir su tamaño y facilitar la cirugía o después de la misma, para limpiar la zona de la cirugía de las posibles células tumorales que hayan podido quedar. Asimismo, se puede administrar con la quimioterapia para potenciar sus efectos (quimioirradiación).
El tratamiento con radioterapia siempre es individualizado, es decir, cada enfermo tendrá su tratamiento específico y distinto al de otro paciente.
En el cáncer de pulmón la utilización de la radioterapia varía en función del tipo de cáncer:
- En los cánceres de pulmón no microcíticos, la radioterapia se utiliza cuando es imposible realizar la cirugía por el riesgo que supone para el paciente, el tumor es inoperable o como tratamiento de algunas metástasis. Puede combinarse con quimioterapia.
- En los carcinomas microcíticos, la radioterapia se utiliza como tratamiento complementario a la quimioterapia en los casos en que la enfermedad está localizada. También está indicada en la prevención y tratamiento de metástasis cerebrales.
Según la finalidad con que se emplee, la radioterapia puede ser curativa o paliativa para aliviar síntomas provocados por el cáncer de pulmón o las metástasis. Este es el caso de la radioterapia antiálgica, utilizada en las lesiones óseas con el objetivo de disminuir el dolor que producen al paciente.
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como el corazón, la medula espinal, las cabezas humerales, el hígado, el estomago, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..
Radioterapia internaEs una técnica de tratamiento que consiste en introducir en el interior del organismo isótopos radiactivos. Se pueden implantar de forma temporal o permanente en la zona a tratar.
Con la radioterapia interna se logra administrar altas dosis de radiación a cortas distancias, de tal forma, que llega muy poca dosis a los tejidos sanos circundantes al implante.
¿Cómo se colocan los implantes? Dependiendo del tipo de implante que se vaya a realizar es necesario permanecer ingresado en el hospital durante 1 o dos días, en otros casos el paciente podrá irse a su casa el mismo día tras recibir el tratamiento. Bajo sedación o anestesia general, se efectuará la colocación de los isótopos radiactivos.
¿Es necesario permanecer aislado? En ocasiones, mientras tenga colocados los implantes es necesario que permanezca en una habitación, preparada especialmente para tal fin.
El paciente estará controlado, en todo momento, a través de un monitor de televisión por el personal sanitario responsable de su cuidado.
¿Cuánto dura el tratamiento? La duración del tratamiento dependerá en gran medida del tipo de isótopo que se haya empleado en el implante y de la cantidad de dosis que se quiera administrar en la zona del tumor, pero generalmente oscila entre minutos y días.
-
R
- Recto (Cáncer)
Cáncer que se forma en los tejidos del recto (las últimas pulgadas del intestino grueso más cercanas al ano).
El recto se sitúa en la pelvis, como se ha mencionado antes.El crecimiento de un tumor originado en esta zona anatómica será tanto hacia la luz o zona “hueca” del recto, como hacia fuera, traspasando las paredes del recto y llegando a los tejidos vecinos.
El drenaje linfático del recto es bastante diferente al de colon. El drenaje linfático del recto va, principalmente, hacia los ganglios perirrectales y paravertebrales.
Por último el tumor también se puede extender por los vasos sanguíneos dando lugar a metástasis en órganos distantes. En el cáncer de recto son más frecuentes las metástasis en el pulmón, a diferencia de lo que ocurre en el cáncer de colon.
El adenocarcinoma es el tipo de tumor más frecuente en el recto. Representa el 95% de los tumores que asientan en esta localización anatómica.
Al igual que en el cáncer de colon, el adenocarcinoma se puede clasificar en tres grados histológicos:- Bien diferenciado.
- Moderadamente diferenciado.
- Escasamente diferenciado.
Otros tipos histológicos mucho más infrecuentes (menos del 5% de los tumores en el recto) son:- Carcinoma de células pequeñas.
- Carcinoma escamoso.
- Carcinoma adenoescamoso.
Actualmente un 44% de los pacientes se diagnostican en estadios iniciales o localizados, un 40% ya con afectación locorregional o locálmente avanzados y solamente un 16% en estadios avanzados o metastático. Estos datos son ligeramente mejores que los observados en el cáncer de colon.
La Clasificación del tumor por Estadios se llama Clasificación TNM y está mundialmente aceptada. La clasificación para el cáncer de recto es igual a la del cáncer de Colon.
La T se refiere al nivel de extensión del tumor primario en las paredes del intestino:
- Tis: es el tumor “in situ”, confinado a la mucosa, que no traspasa las capas de la mismo.
- T1: tumor que invade la submucosa.
- T2: tumor que invade la muscularis propia.
- T3: tumor que llega hasta la subserosa o los tejidos grasos perirectales.
- T4: tumor que invade tejidos de órganos adyacentes, como la vejiga urinaria, próstata, vagina o útero).
La N se refiere a la presencia o no de afectación de los ganglios linfáticos
regionales o más próximos a la zona donde se origina el tumor.
- N0: significa ausencia de afectación ganglionar.
- N1: significa la presencia de afectación tumoral en 1 a 3 glánglios linfáticos perirectales
- N2: significa metástasis o afectación de 4 o más ganglios linfáticos.
La M se refiere a la presencia confirmada de metástasis a distancia:
- M0: es ausencia de metástasis
- M1: es presencia de metástasis a distancia.
Estadio 0 Tis N0 M0 Estadio I T1-2 N0 M0 Estadio IIA T3 N0 M0 Estadio IIB T4 N0 M0 Estadio IIIA T1-2 N1 M0 Estadio IIIB T3-4 N1 M0 Estadio IIIC Cualquier T N2 M0 Estadio IV Cualquier T Cualquier N M1
Eleccion de Tratamiento
Dependerá, fundamentalmente, del estadio clínico de la enfermedad tumoral.
De forma resumida se puede decir que en los tumores muy localizados (estadios 0 y I) el tratamiento fundamental es la cirugía. Se debe resecar el tumor con un margen de tejido sano periférico de, al menos, 1 cm. Aún así las recurrencias locales son frecuentes (50% de los casos) pero se pueden tratar de nuevo con cirugía.
Los estadios localmente avanzados (Estadios II y IIIA) deben de tratarse con una combinación de tipos de tratamiento. Lo más recomendable, según los estudios más recientes, es realizar primero un tratamiento con radioterapia y quimioterapia simultáneas (lo que se llama tratamiento quimio-radioterápico neoadyuvante) seguido de una cirugía radical. Las posibilidades de mejorar la supervivencia global son, de este modo, muy significativas.
Los estadios IIIB y IV tienen pocas posibilidades de curación a largo plazo con los tratamientos actualmente conocidos. La quimioterapia y la radioterapia son los tipos de tratamiento más importantes.
Estadio 0 (carcinoma in situ)
El tratamiento para el estadio 0 puede incluir los siguientes procedimientos:
- Polipectomía simple.
- Escisión local.
- Resección. (Cuando el tumor es muy grande para extirparlo mediante escisión local).
- Radioterapia interna o externa.
Cáncer de recto en estadio I
El tratamiento del cáncer de recto en estadio I puede incluir los siguientes procedimientos:
- Escisión local.
- Resección.
- Resección, con radioterapia y quimioterapia antes o después de la cirugía.
Cáncer de recto en estadio II
El tratamiento del cáncer de recto en estadio II puede incluir los siguientes procedimientos
- Resección, más una combinación de quimioterapia y radioterapia antes o después de la cirugía.
Cáncer de recto en estadio III
El tratamiento del cáncer de recto en estadio III puede incluir los siguientes procedimientos:
- Resección, más una combinación de quimioterapia y radioterapia antes o después de la cirugía.
Cáncer de recto en estadio IV y recidivante
El tratamiento del cáncer de recto en estadio IV y el cáncer de recto recidivante puede incluir los siguientes procedimientos:
- Resección, con una combinación de radioterapia y quimioterapia antes de la cirugía.
- Resección o exenteración pélvica como tratamiento paliativo para aliviar los síntomas y mejorar la calidad de vida.
- Radioterapia, quimioterapia o una combinación de ambas como tratamiento paliativo para aliviar los síntomas y mejorar la calidad de vida.
- Quimioterapia para controlar el crecimiento del tumor.
- Colocación de una cánula para ayudar a mantener abierto el recto si el tumor lo bloquea parcialmente, como tratamiento paliativo para aliviar los síntomas y mejorar la calidad de vida.
El tratamiento del cáncer de recto que se diseminó hasta otros órganos depende del órgano hasta donde el cáncer se diseminó.- Quimioterapia regional o sistémica.
- Radioterapia interna.
- Cirugía para extirpar el tumor, con quimioterapia o sin ella antes de la cirugía.
El tratamiento de las áreas del cáncer que se diseminó hasta el pulmón o los ovarios es cirugía.
Quimioterapia
La quimioterapia es un tratamiento del cáncer que utiliza medicamentos para interrumpir el crecimiento de células cancerosas, mediante su destrucción o evitando su multiplicación. Cuando la quimioterapia se administra oralmente o se inyecta en una vena o músculo, los medicamentos ingresan al torrente sanguíneo y afectan a células cancerosas en todo el cuerpo (quimioterapia sistémica).
Cuando la quimioterapia se coloca directamente en la columna vertebral, un órgano o una cavidad corporal como el abdomen, los medicamentos afectan principalmente células cancerosas de esas áreas (quimioterapia regional).
La forma en que se administra la quimioterapia depende del tipo y el estadio del cáncer que se está tratando.
Cirugia
En el pasado se pensaba que la cirugía era el tratamiento de elección.
Sin embargo, la mayoría de estas intervenciones implicaba eliminar todo el esfínter anal, lo que originaba una incontinencia fecal permanente y conllevaba la realización de una colostomía (abocar el tubo digestivo directamente a la pared abdominal para la eliminación de las heces).
Actualmente se puede evitar esta cirugía amputadora, en muchos casos, con la radioterapia y la quimioterapia prequirúrgicas.
Radioterapia
La radioterapia es un tratamiento que utiliza rayos X de alta energía u otros tipos de radiación para destruir células cancerosas.
Hay dos tipos de radioterapia.
La radioterapia externa utiliza una máquina fuera del cuerpo que envía la radiación hacia cáncer.
La radioterapia interna utiliza una sustancia radiactiva sellada en agujas, semillas, cables o catéteres que se colocan directamente en el cáncer o cerca del mismo.
La forma en que se administre la radioterapia depende del tipo y el estadio del cáncer que se está tratando.
Planificación del tratamiento con RT:Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como la vejiga, las cabezas femorales, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..
Radioterapia internaEs una técnica de tratamiento que consiste en introducir en el interior del organismo isótopos radiactivos. Se pueden implantar de forma temporal o permanente en la zona a tratar.
Con la radioterapia interna se logra administrar altas dosis de radiación a cortas distancias, de tal forma, que llega muy poca dosis a los tejidos sanos circundantes al implante.
¿Cómo se colocan los implantes?Dependiendo del tipo de implante que se vaya a realizar es necesario permanecer ingresado en el hospital durante 1 o dos días, en otros casos el paciente podrá irse a su casa el mismo día tras recibir el tratamiento. Bajo sedación o anestesia general, se efectuará la colocación de los isótopos radiactivos.
¿Es necesario permanecer aislado?En ocasiones, mientras tenga colocados los implantes es necesario que permanezca en una habitación, preparada especialmente para tal fin.
El paciente estará controlado, en todo momento, a través de un monitor de televisión por el personal sanitario responsable de su cuidado.
¿Cuánto dura el tratamiento?La duración del tratamiento dependerá en gran medida del tipo de isótopo que se haya empleado en el implante y de la cantidad de dosis que se quiera administrar en la zona del tumor, pero generalmente oscila entre minutos y días.
- Riñon (Cáncer)
- Cáncer que se forma en tejidos de los riñones. El cáncer de riñón comprende el carcinoma de células renales (cáncer que se forma en el recubrimiento de tubos muy pequeños del riñón que filtran la sangre y eliminan los productos de desperdicio) y el carcinoma de la pelvis renal (cáncer que se forma en el centro del riñón donde se acumula la orina). También comprende el tumor de Wilms, que es un tipo de cáncer de riñón que suele desarrollarse en niños menores de 5 años de edad.
El cáncer de riñón, también llamado hipernefroma, puede curarse con una operación quirúrgica cuando está localizado. Sin embargo cuando el tumor se ha extendido a otros lugares (metástasis), el pronóstico en general es muy desfavorable, aunque un pequeño porcentaje de pacientes pueden tener una lenta evolución durante varios años.
El cáncer de riñón es uno de los pocos tumores, en los que se han descrito, de forma excepcional, regresiones espontáneas.
Una vez que se ha diagnosticado el cáncer, se hacen pruebas para determinar si el cáncer se ha diseminado fuera del riñón a otras partes del cuerpo y poder planificar el tratamiento más adecuado.
El cáncer renal se clasifica en varios estadios en función de la extensión local del tumor, de su extensión regional (número y tamaño de los ganglios linfáticos cercanos al riñón) y de su extensión a distancia o metástasis.
En función de estos parámetros el tumor se clasifica en varios estadios que se utilizan para establecer el pronóstico y el tipo de tratamiento que es necesario. El tratamiento quirúrgico puede curar a más del 50% de los pacientes con enfermedad en estadio I, mientras que las terapias obtienen resultados muy pobres en el estadio IV.
Estadio I:El cáncer está limitado en riñón y mide menos de 7 cm.
Estadio II:El cáncer está limitado en riñón y mide más de 7 cm.
Estadio III:El cáncer invade a los ganglios cerca del riñón, o invade las estructuras que se hallan alrededor del riñón (glándula suprarrenal, grandes vasos sanguíneos adyacentes).
Estadio IV:El cáncer invade a varios ganglios estén cerca o no del riñón, y están afectados órganos lejanos.
En esta situación, se suelen utilizar otras clasificaciones que intentan proporcionar información acerca del pronóstico (como la clasificación de Motzer), distinguiendo tres grupos: mal, intermedio y buen pronóstico.El cáncer de riñón en niñosEl cáncer en los niños es muy poco frecuente.
En esta población el tumor de riñón se debe a alteraciones de los genes y se denomina Tumor de Wilms. Afortunadamente la mayoría de estos niños se pueden curar, con tratamientos multidisciplinarios y en centros especializados.
En ocasiones (uno de cada diez niños) se asocian a malformaciones genéticas o retraso mental.
Hay otros tipos de tumores renales en niños, diferente al tumor de Wilms, cuya incidencia es afortunadamente muy baja (tumores de células claras, tumores rabdoides, tumores neuroepiteliales y el nefroblastoma quístico).
Elección del tratamiento
En la actualidad, se dispone de varios tipos de tratamiento para los pacientes con cáncer de riñón:- Cirugía
- Radioterapia
- Terapia Biológica
- Quimioterapia
- Terapia dirigida contra dianas específicas
De todos ellos, solo la cirugía puede considerarse un tratamiento estandar para tumores localizados en los que es posible la curación de la enfermedad en más del 50% de los casos.El resto de tratamientos deben considerarse en el contexto de tratamientos paliativos o experimentales y deben estar sometidos a ensayos clínicos en pacientes con enfermedad locorregional y/o con metástasis a distancia.
Los pacientes con tumores localmente avanzados y/o metastásicos deberian, a ser posible, participar en ensayos clínicos.
Cáncer de células renales en estadio IEl tratamiento del cáncer de células renales en estadio I puede incluir los siguientes procedimientos:- Cirugía (nefrectomía radical, nefrectomía simple o nefrectomía parcial).
- Radioterapia como terapia paliativa para aliviar los síntomas de los pacientes que no se pueden someter a cirugía.
- Embolización arterial como terapia paliativa.
Cáncer de células renales en estadio IIEl tratamiento para el cáncer de células renales en estadio II puede incluir los siguientes procedimientos:- Cirugía (nefrectomía radical o nefrectomía parcial).
- Cirugía (nefrectomía), antes de la radioterapia o después de ella.
- Radioterapia como terapia paliativa para aliviar los síntomas de los pacientes que no se pueden someter a cirugía.
- Embolización arterial como terapia paliativa.
Cáncer de células renales en estadio IIIEl tratamiento contra el cáncer de células renales en estadio III puede incluir los siguientes procedimientos:- Cirugía (nefrectomía radical). También se pueden extraer vasos sanguíneos del riñón y algunos ganglios linfáticos.
- Embolización arterial seguida de cirugía (nefrectomía radical).
- Radioterapia como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
- Embolización arterial como terapia paliativa.
- Cirugía (nefrectomía) como terapia paliativa.
- Radioterapia antes de la operación o después de ella (nefrectomía radical).
Cáncer de células renales en estadio IV y recidivanteEl tratamiento para el cáncer de células renales en estadio IV y recidivante puede incluir los siguientes procedimientos:- Terapia dirigida sola o después de la terapia biológica.
- Terapia biológica sola o después de la cirugía (nefrectomía) para reducir el tamaño del tumor.
- Embolización arterial como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
- Radioterapia como tratamiento paliativo para aliviar los síntomas y mejorar la calidad de vida.
- Cirugía (nefrectomía) como terapia paliativa.
- Cirugía (nefrectomía radical con extirpación del cáncer de otras áreas donde se diseminó o sin extirpación).
CirugíaLa resección quirúrgica es el tratamiento más utilizado en esta enfermedad.
El cáncer de riñón puede curarse con una operación cuando está localizado (estadio I).
En estadios avanzados la cirugía puede ayudar a paliar los síntomas provocados por el tumor y en algunos pacientes con poca enfermedad metastásica se puede obtener mayor supervivencia si se realiza exéresis del tumor y de las metástasis
En la operación puede que se extirpe solo el riñón (nefrectomía simple) o que sea necesario extirpar los tejidos adyacentes (nefrectomía radical, que incluye el riñón, la glándula suprarrenal y los ganglios linfáticos).
Se puede vivir con un solo riñón funcionante sin problemas importantes.
Si el tumor está localizado pero no se puede operar, se puede intentar paliar los síntomas que ocasiona mediante radioterapia o mediante la obstrucción selectiva de los vasos sanguíneos que lo sustentan (embolización).
Quimioterapia
La quimioterapia es un tratamiento de fármacos para eliminar las células tumorales. Los tumores del riñón son, generalmente, resistentes a los tratamientos de quimioterapia. En el momento actual, suelen usarse en situaciones donde existe un componente tumoral en forma de sarcoma.
La quimioterapia se considera un tratamiento sistémico ya que el medicamento es introducido al torrente sanguíneo, viaja a través del cuerpo y puede eliminar las células cancerosas que estén fuera del riñón.
Radioterapia
La radioterapia es un tratamiento que se utiliza para eliminar células tumorales y disminuir el tamaño del tumor
En pacientes inoperables la radioterapia puede ayudar a paliar los síntomas producidos por el tumor primario o por las metástasis (por ejemplo, dolor por afectación ósea o de nervios).
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como el riñon contralateral, el hígado, el bazo, el estomago, la medula espinal, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..
-
S
- Sarcomas de partes blandas (Cáncer)
Durante el desarrollo gestacional, se forman nuestros tejidos y nuestros órganos a partir de una de las 3 capas embrionarias, denominadas ectodermo, mesodermo y endodermo.
Del mesodermo se van a formar determinados tejidos como los músculos, los tejidos cartilaginosos, las articulaciones, los huesos, los tejidos conectivos (por ejemplo los tendones), los vasos saguineos y linfáticos y los tejidos grasos. Estos tejidos a su vez están formados por células, que se dividen de forma regular con el fin de reemplazar a las ya envejecidas o muertas y mantener así la integridad y el correcto funcionamiento de los cuerpo.Este proceso está regulado por una serie de mecanismos que indican a la célula cuándo comenzar a dividirse y cuándo permanecer estable. Cuando estos mecanismos se alteran en una célula, ésta y sus descendientes inician una división incontrolada que con el tiempo dará lugar a un tumor.
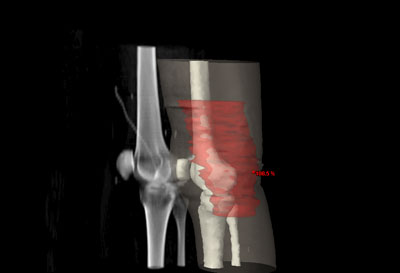
Llamamos sarcoma de partes blandas, a aquella enfermedad en la que se desarrollan células malignas a partir de alguna de las células que derivan del mesodermo, a excepción del hueso (en este caso no hablaríamos de Sarcomas de partes blandas, sino de Osteosarcomas).
Los sarcomas de partes blandas pueden aparecer en los tejidos mesodérmicos de las extremidades (más de la mitad de los casos), del tronco y del abdomen e incluso del cuello y la cabeza.
En ocasiones los sarcomas surgen en tracto gastrointestinal; en ese caso hablamos de un tipo de sarcoma muy especial, muy diferente al resto tanto en su crecimiento, pronóstico y tratamiento. Estos tumores originados del tracto gastrointestinal se denominan Sarcomas del Estroma Gastrointestinal (GISTs por sus siglas en inglés) y se publicarán próximamente en esta sección.
Existe tantos tipos de sarcomas de partes blandas, como tipos de células de las que se originan.Nombre Tejido del que derivan
Histiocito mafibroso maligno Tejidos fibrosos Liposarcoma Tejidos grasos Leiomiosarcoma
Células del músculo liso Rabdomiosarcoma Músculo estriado Angiosarcoma
Células que forman los vasos sanguíneos Tumor del estroma
gastrointesinal (GIST)Tracto gastrointestinal
Los más frecuentes son el histiocitoma fibroso maligno seguido del liposarcoma.
Estadio I: En el estadio I, el tumor puede ser de cualquier tamaño, de grado bajo (probablemente de crecimiento y diseminación lenta), y puede ser superficial (próximo a la superficie de la piel) o profundo.
Estadio II: En el estadio II, el tumor es de grado alto (probablemente de crecimiento y diseminación rápida) y ya sea:- de 5 centímetros o menos y puede ser superficial (próximo a la superficie de la piel) o profundo; o
- de 5 centímetros o más y superficial.
Estadio III: En el estadio III, el tumor es de grado alto, mayor de 5 centímetros y profundo.
Estadio IV: En el estadio IV, el tumor puede ser de cualquier tamaño, cualquier grado y se ha diseminado a los ganglios linfáticos circundantes o a otras partes del cuerpo.
Tratamiento
El tratamiento de los sarcomas de partes blandas debe de realizarse con un equipo multidisciplinar de médicos, en el que intervienen patólogos, radiólogos, oncólogos médicos, cirujanos y oncólogos radioterapeutas. El tratamiento más adecuado es la cirugía, pero en ocasiones se asocia a radioterapia e incluso a la quimioterapia.
Sarcoma de tejido blando en adultos en estadio l
El tratamiento del sarcoma de tejido blando en adultos en estadio l incluye los siguientes procedimientos:- Cirugía (escisión local amplia o microcirugía de Mohs).
- Radioterapia antes o después de la cirugía.
Si el cáncer se encuentra en la cabeza, el cuello, el abdomen o el pecho, el tratamiento puede incluir los siguientes procedimientos:
- Cirugía.
- Radioterapia antes o después de la cirugía.
- Radioterapia de neutrones rápidos.
Sarcoma de tejido blando en adultos en estadios Il y lllEl tratamiento del sarcoma de tejido blando en adultos en estadios ll y lll incluye los siguientes procedimientos:
- Cirugía (escisión local amplia).
- Cirugía (escisión local amplia) con radioterapia para tumores grandes.
- Radioterapia de dosis alta para los tumores que no pueden extirparse mediante cirugía.
- Radioterapia o quimioterapia antes de aplicar cirugía preservadora del miembro. La radioterapia también puede administrarse después de la cirugía.
Sarcoma de tejido blando en adultos en estadio IVEl tratamiento del sarcoma de tejido blando en adultos en estadio lV con implicación de los ganglios linfáticos puede incluir los siguientes procedimientos:
- Cirugía (con escisión local amplia) con linfadenectomía o sin esta. También se puede administrar radioterapia después de la cirugía.
- Radioterapia antes y después de la cirugía seguida de quimioterapia.
El tratamiento del sarcoma de tejido blando en estadio IV con compromiso de los órganos internos del cuerpo puede incluir los siguientes procedimientos:
- Cirugía (escisión local amplia).
- Cirugía para extirpar la mayor cantidad posible de tumor, seguida de radioterapia.
- Radioterapia de dosis alta, con quimioterapia o sin esta, para tumores que no pueden extirparse mediante cirugía.
- Quimioterapia con uno o más medicamentos contra el cáncer, antes de la cirugía, o como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
Estos tratamientos pueden ser seguidos de cirugía para extirpar lesiones en los pulmones.
Opciones de tratamiento para el sarcoma de tejido blando en adultos recidivante
El tratamiento para el sarcoma de tejido blando en adultos recidivante puede incluir los siguientes procedimientos:
- Cirugía (escisión local amplia) con radioterapia antes o después de la cirugía.
- Cirugía (amputación).
- Radioterapia seguida de cirugía preservadora del miembro.
- Cirugía para extirpar el cáncer que recidivó en el pulmón.
- Quimioterapia con uno o más medicamentos contra el cáncer.
Cirugía
El tratamiento ideal consiste en una cirugía con márgenes amplios, al menos con 2 centímetros.
Los cirujanos siempre valoran realizar operaciones con vistas a la curación, dentro de un marco de cirugías conservadoras, es decir con cirugías que no sean muy mutilantes (por ejemplo evitar amputaciones). Para lograr estos objetivos a veces se utiliza la quimioterapia o la radioterapia antes de la cirugía. La cirugía también tiene un valor en enfermos con metástasis; existen algunos pacientes con tumores metastáticos que pueden llegar a curarse cuando hay pocas metástasis y éstas se pueden extirpar.
Quimioterapia
La quimioterapia es un tratamiento de fármacos para eliminar las células tumorales. La quimioterapia se considera un tratamiento sistémico ya que el medicamento es introducido al torrente sanguíneo, viaja a través del cuerpo y puede eliminar las células cancerosas que estén lejos del origen inicial.
Los fármacos utilizados en la quimioterapia pueden:- Administrarse en la sangre (quimioterapia intravenosa)
- Con pastillas (quimioterapia oral).
La quimioterapia puede tener un papel en una de estas tres situaciones:
- Después de la cirugía, en ese caso se llama quimioterapia adyuvante
- Antes de la cirugía con idea de disminuir el tamaño tumoral y evitar la diseminación temprana del tumor, en ese caso se llama quimioterapia neoadyuvante
- Bien como paliación cuando hay metástasis irresecables, en ese caso se llama quimioterapia paliativa.
La quimioterapia adyuvante se aplica después de la cirugía y en el caso de que el tumor sea de mal pronóstico, como es el caso de los tumores de alto grado o los tumores mayores de 5 centímetros. Los tumores de bajo grado no necesitan este tratamiento. La quimioterapia neoadyuvante tiene la misión de facilitar la cirugía, potencialmente curativa, posterior. Si un paciente presenta un sarcoma con metástasis que no puede operarse, entonces se pueden paliar los síntomas con quimioterapia.
Radioterapia
La radioterapia se utiliza cuando el tumor no se puede extirpar por que esta muy profundo o en una localización que lo hace inoperable. En ocasiones esta radioterapia puede favorecer que, en un segundo tiempo, se pueda operar. La radioterapia también se utiliza cuando los márgenes obtenidos después de la cirugía no son suficientes.
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar. Los más empleados son una máscara de material termoplástico que se adapta al contorno del paciente.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control.-
T
- Testículo (Cáncer)
- Cáncer que se forma en los tejidos del testículo (uno de las dos glándulas con forma de huevo que se encuentran adentro del escroto y producen el esperma y las hormonas masculinas). Por lo general, el cáncer de testículo se presenta en hombres jóvenes y de mediana edad. Los dos principales tipos de cáncer de testículo son los seminomas (cánceres que crecen lentamente y son sensibles a la radioterapia) y los no seminomas (distintos tipos de células que crecen más rápidamente que los seminomas).
El cáncer de testículo es un tumor aparece sobre todo en hombres jóvenes y, generalmente es de buen pronóstico. Incluso los estadios más avanzados pueden ser curables, con cirugía y quimioterapia y/o radioterapia. Es el cáncer más común en hombres jóvenes, de 15 a 35 años de edad. En España, la incidencia anual se sitúa entre 1,6 y 2 casos por cada 100.000 habitantes
Desde un punto de vista del pronóstico, posibilidad de ocasionar metástasis y de la planificación del tratamiento, el cáncer de testículo se divide en dos tipos seminoma y no seminoma.
Los seminoma son tumores de células germinales inmaduras de crecimiento lento y representan alrededor del 50% de los casos, de los cuales el 75% son de estadio 1. Los seminomas tienden a estar confinados al testículo puesto que se propagan relativamente despacio, y a través del sistema linfático. Suelen ser los más habituales entre el segmento de pacientes de mayor edad.
Los no seminoma, por el contrario, son células germinales más maduras que se propagan con mayor rapidez. Los noseminomas engloban a varios subtipos; pero se tratan de forma similar:- Carcinoma embrionario, es es tipo más común, aunque normalmente aparece junto con otros tipos.
- Tumor de saco vitelino, es el tipo más común en los niños, en los que se cura con mucha más facilidad que en los adultos.
- Coriocarcinoma, es un tipo muy poco frecuente (1%). Dado su extensión por la sangre, es uno de los subtipos más agresivos.
- Teratoma inmaduro
- Teratoma maduro, son células adultas premalignas que rara vez se extienden, pero que pueden transformarse en otro tipo.
Los pacientes con seminoma tienen un pronóstico excelente: la tasa de curaciones globalmente es del 90%, e incluso en los estadios más iniciales es cercana al 100%.
En caso de tumores mixtos, que se da la mitad de las veces (Seminoma y No-Seminoma) el tumor deberá ser tratado si fuera un tumor no seminoma.
Etapas del tumor
Una vez que se ha diagnosticado el cáncer, se hacen pruebas para determinar si el cáncer se ha diseminado del testículo a otras partes del cuerpo y poder planificar el tratamiento más adecuado.
El cáncer de testículo se clasifica en varios estadios en función de la presencia de:- Marcadores tumorales elevados.
- La extensión local del tumor (grado de invasión de las estructuras alrededor del testículo, por ejemplo el cordón espermático o el escroto).
- Su extensión regional (número y tamaño de los ganglios linfáticos cercanos al testículo, por ejemplo inguinales).
- Su extensión a distancia o metástasis.
En función de estos parámetros el tumor de testículo se clasifica en varios estadios que se utilizan para establecer el pronóstico y el tipo de tratamiento que es necesario.
Estadio I: El cáncer está limitado al testículo.
Estadio II: El cáncer incluye el testículo y los ganglios linfáticos cercanos al testículo.
Estadio III: El cáncer invade más allá de los ganglios cercanos al testículo.
Estadio IV: Hay metástasis en otros órganos.
Opciones de Tratamiento
Cáncer de la testiculo en estadio I
El tratamiento del cáncer de testículo en estadio I depende de si el cáncer es un seminoma o un no seminoma.
El tratamiento del seminoma puede incluir los siguientes procedimientos:- Cirugía para extirpar el testículo, con radioterapia dirigida a los ganglios linfáticos del abdomen después de la cirugía, con seguimiento durante toda la vida.
- Cirugía para extirpar el testículo, seguida de quimioterapia y seguimiento durante toda la vida.
El tratamiento del no seminoma puede incluir los siguientes procedimientos:- Cirugía para extirpar el testículo y los ganglios linfáticos del abdomen, con seguimiento durante toda la vida.
- Cirugía para extirpar el testículo, con seguimiento durante toda la vida.
- Cirugía seguida por quimioterapia para los pacientes con riesgo alto de recidiva, con seguimiento durante toda la vida.
Cáncer de la testiculo en estadio II
El tratamiento del cáncer de testículo en estadio II depende de si el cáncer es un seminoma o un no seminoma.
El tratamiento del seminoma puede incluir los siguientes procedimientos:- Cuando el tumor mide cinco centímetros o menos, el tratamiento habitual es cirugía para extirpar el testículo seguida de radioterapia dirigida a los ganglios linfáticos del abdomen y la pelvis, con seguimiento permanente.
- Cuando el tumor mide más de cinco centímetros, el tratamiento habitual es cirugía para extirpar el testículo seguida de quimioterapia de combinación o radioterapia dirigida a los ganglios linfáticos del abdomen y la pelvis, con seguimiento durante toda la vida.
El tratamiento del no seminoma puede incluir los siguientes procedimientos:- Cirugía para extirpar el testículo y los ganglios linfáticos, con seguimiento durante toda la vida.
- Cirugía para extirpar el testículo y los ganglios linfáticos, seguida de quimioterapia de combinación y seguimiento durante toda la vida.
- Cirugía para extirpar el testículo, seguida por quimioterapia de combinación y una segunda cirugía si el cáncer permanece, con seguimiento durante toda la vida.
- Quimioterapia de combinación antes de la cirugía para extirpar el testículo en el caso del cáncer que se diseminó y se considera potencialmente mortal.
Cáncer de la testiculo en estadio III
El tratamiento del cáncer de testículo en estadio III depende de si el cáncer es un seminoma o un no seminoma.
El tratamiento del seminoma puede incluir los siguientes procedimientos:- Cirugía para extirpar el testículo, seguida de quimioterapia de combinación. Cualquier tumor que quede después del tratamiento necesitará seguimiento durante toda la vida.
El tratamiento del no seminoma puede incluir los siguientes procedimientos:- Cirugía para extirpar el testículo, seguida de quimioterapia de combinación.
- Quimioterapia de combinación seguida por cirugía para extirpar todo tumor que haya quedado. Se puede administrar quimioterapia adicional si el tejido del tumor extirpado contiene células cancerosas en crecimiento.
- Quimioterapia de combinación con radioterapia dirigida al cerebro en el caso del cáncer que se diseminó hasta el cerebro.
- Quimioterapia de combinación antes de la cirugía para extirpar el testículo en el caso del cáncer que se diseminó y se considera potencialmente mortal.
Opciones de tratamiento para el cáncer de testículo recidivante
El tratamiento del cáncer de testículo recidivante puede incluir los siguientes procedimientos:- Quimioterapia de combinación.
- Dosis alta de quimioterapia con trasplante de médula ósea.
- Cirugía para extirpar el cáncer que: volvió más de dos años después de la remisión completa; o volvió a un solo lugar y no responde a la quimioterapia.
Cirugía
La cirugía con la idea de curar el cáncer de testículo consiste en la extirpación del testículo a través de una incisión en la ingle (este procedimiento se denomina Orquiectomía radical).
A diferencia de otros tipos de tumores en el cáncer de testículo no está recomendado la cirugía directa (es decir a través de una pequeña incisión en el escroto), para evitar el riesgo de diseminación del tumor hacia el escroto o hacia los ganglios linfáticos.
En algunas ocasiones es necesaria la cirugía en ganglios linfáticos o en lesiones “sospechosas” alejadas del tumor original.
El tratamiento administrado después de la cirugía, con el propósito de aumentar las posibilidades de curación, se denomina tratamiento adyuvante.
Quimioterapia
La quimioterapia es un tratamiento de fármacos para eliminar las células tumorales. La quimioterapia se considera un tratamiento sistémico ya que el medicamento es introducido al torrente sanguíneo, viaja a través del cuerpo y puede eliminar las células cancerosas que estén fuera del testículo.
La quimioterapia es el tratamiento estándar, con o sin radiación, cuando el cáncer se ha extendido a otras partes del cuerpo (o sea, estadio 2 ó 3). En algunos sitios se ofrece como opción para los tumores testiculares que tienen algún factor de mal pronóstico (afectación de los vasos sanguíneos o por el tamaño tumoral) en estadio 1 como terapia preventiva en los casos de mayor riesgo. La introducción de la terapia con cisplatino como agente antitumoral supuso una revolución espectacular en la tasa de curación de este tipo de cáncer. Los agentes más utilizados son el cisplatino, etóposido y bleomicina. Los fármacos antitumorales causan efectos secundarios importantes, tanto agudos (vómitos, náuseas, caída del pelo, cansancio, neutropenia, sépsis, azooespermia), como a largo plazo (ototoxicidad, neuropatía periférica, tumores secundarios, problemas cardiovasculares).
Aunque el éxito del tratamiento depende del estadio, la tasa media de supervivencia (a cinco años) es de alrededor del 95%, y para los casos de cánceres en estadio 1 (si son vigilados adecuadamente) es de prácticamente el 100% de supervivencia. Por eso es de suma importancia la acción inmediata cuando existe la posibilidad de padecer cáncer de testículo.
La quimioterapia es una de las modalidades terapéuticas más empleada en el tratamiento del cáncer.
Radioterapia
La radioterapia mediante rayos X de alta energía es efectiva en los tumores germinales. Se puede administrar para tratar seminomas de estadio 2, o como terapia preventiva en el caso de cáncer en estadio 1, y así minimizar la probabilidad de que aún existan tumores minúsculos indetectables y que pudiesen extenderse. La extraordinaria sensibilidad a la radioterapia de los seminomas hace que la tasa de curación para los casos en estadio 1 sea superior al 95%.
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como las cabezs femorales, intestino delgado, vejiga, recto, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control. - Tiroides (Cáncer)
Cáncer que se forma en la glándula tiroidea (un órgano ubicado en la base de la garganta que produce hormonas que ayudan a controlar la frecuencia cardíaca, la presión arterial, la temperatura del cuerpo y el peso). Los cuatro tipos más importantes de cáncer de tiroides son el papilar, el folicular, el medular y el anaplásico. Los cuatro tipos se determinan de acuerdo con el aspecto de las células bajo un microscopio.
Hay cuatro tipos diferentes de cáncer de tiroides, los cuales presentan un comportamiento muy diferente.
- Carcinoma papilar de tiroides: representa el 80-85% de los cánceres de tiroides. Se originan a partir de las células foliculares del tiroides. Crecen muy lentamente aunque puede afectar a los ganglios linfáticos. Tiene muy buen pronóstico.
- Carcinoma folicular de tiroides: representa el 5-10% de los cánceres de tiroides. Se originan a partir de las células foliculares o de las células de Hurthle del tiroides. Es más frecuente en aquellas áreas donde hay déficit de yodo en la alimentación. Suele tener un buen pronóstico.
- Carcinoma medular de tiroides: representa el 5% de los cánceres de tiroides. Se originan a partir de las células C del tiroides. Producen aumento de una hormona característica denominada calcitonina que está relacionada con la regulación de los niveles de calcio. En el 80% de los casos no se asocia a ningún síndrome hereditario, no relacionándose con ningún factor de riesgo. En el otro 20% de los carcinomas medulares de tiroides son consecuencia de un gen anormal, originando un síndrome de carcinoma medular de tiroides familiar. La combinación de este síndrome con tumores de otras glándulas endocrinas se conoce como neoplasia endocrina múltiple tipo 2 (MEN 2). Pídale información a su médico sobre los análisis de sangre y sobre las pruebas genéticas.
- Carcinoma anaplásico de tiroides: es un cáncer de tiroides muy poco frecuente. Es muy agresivo y su pronóstico es malo.
Elección del Tratamiento
Una vez que se ha confirmado el diagnóstico de cáncer de tiroides, y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado para curarla. El especialista recomendará y explicará las posibilidades de tratamiento más óptimas en cada caso, para que el paciente con toda la información pueda junto con el médico tomar una decisión.
En el tratamiento del cáncer de tiroides se sigue un protocolo, es decir un conjunto de normas y pautas (plan de tratamiento), establecidas en base a la experiencia científica que se tiene en el tratamiento de este tumor.
Estos protocolos, que se emplean de forma generalizada en todos los hospitales, recogen las indicaciones o limitaciones del tratamiento en función de los siguientes factores:
- Fase o estadio en la que se encuentra la enfermedad (TNM).
- Tipo de tumor
- Características del paciente: edad, enfermedades que dificulten algún tratamiento específico, estado nutricional…
Cáncer de tiroides papilar y folicular en estadio I y II
El tratamiento del cáncer de tiroides papilar y el cáncer de tiroides folicular en estadios I y II puede incluir los siguientes procedimientos:
- Tiroidectomía total o casi total, con tratamiento con yodo radiactivo o sin este.
- Lobectomía y extirpación de los ganglios linfáticos que contienen cáncer, seguida de terapia con hormonas. Se puede administrar yodo radiactivo después de la cirugía.
Cáncer de tiroides papilar y folicular en estadio III
El tratamiento del cáncer de tiroides papilar y el cáncer de tiroides folicular en estadio III es habitualmente tiroidectomía total. También se puede extirpar el cáncer que se diseminó por afuera de la tiroides, así como los ganglios linfáticos que contienen cáncer. Se puede administrar yodo radiactivo o radioterapia externa después de la cirugía.
Cáncer de tiroides papilar y folicular en estadio IV
El cáncer de tiroides papilar y el cáncer de tiroides folicular en estadio IV que se diseminó solo hasta los ganglios linfáticos a menudo se puede curar. Cuando el cáncer se diseminó hasta otras partes del cuerpo como, por ejemplo, los pulmones y los huesos, el tratamiento generalmente no cura el cáncer, pero puede aliviar los síntomas y mejorar la calidad de vida. El tratamiento puede incluir los siguientes procedimientos:
- Tratamiento con yodo radiactivo.
- Radioterapia de haz externo.
- Cirugía para extirpar el cáncer de las áreas hasta donde se diseminó.
- Terapia con hormonas.
Cáncer de tiroides medular
El tratamiento puede incluir los siguientes procedimientos:
- Tiroidectomía total si el cáncer no se diseminó hasta otras partes del cuerpo.
- Extirpación de los ganglios linfáticos que contienen cáncer.
- Radioterapia externa como tratamiento paliativo para aliviar los síntomas y mejorar la calidad de vida de los pacientes cuyo cáncer recidivó en la tiroides.
- Quimioterapia como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida de los pacientes cuyo cáncer se diseminó hasta otras partes del cuerpo.
Cáncer de tiroides anaplásico
El tratamiento puede incluir los siguientes procedimientos:
- Traqueotomía como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
- Tiroidectomía total como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida de los pacientes cuyo cáncer no se diseminó más allá de la tiroides.
- Radioterapia externa.
- Quimioterapia.
Opciones de tratamiento para el cáncer de tiroides recidivante
El tratamiento del cáncer de tiroides recidivante puede incluir los siguientes procedimientos:
- Cirugía, con tratamiento con yodo radiactivo o sin este.
- Tratamiento con yodo radiactivo cuando el cáncer se encuentra solamente mediante una ecografía de la tiroides y no se puede palpar durante un examen físico.
- Radioterapia externa o radioterapia intraoperatoria como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
- Quimioterapia.
Cirugía
La cirugía es el principal tratamiento del cáncer de tiroides.
Hay varios tipos:
- Lobectomía. Operación en la que se extrae sólo el lado de tiroides donde se encuentra el cáncer. Se pueden extraer ganglios linfáticos en el área para determinar si están afectados.
- Tiroidectomía casi total. Operación en la que se extrae todo el tiroides salvo una pequeña parte.
- Tiroidectomía total. Operación en la que se extrae todo el tiroides.
- Disección de ganglios linfáticos. Operación en la que se extraen los ganglios linfáticos en el cuello a los que se ha propagado el cáncer.
Las principales complicaciones de la cirugía del tiroides son: el hipotiroidismo, es decir, una función demasiado baja de la glándula, por lo que es posible que el paciente precise tratamiento oral con hormonas tiroideas de por vida; la parálisis de cuerdas vocales; y la extirpación accidental de las glándulas paratiroides (localizadas detrás de la glándula tiroides), lo que da como resultado una bajada del calcio sanguíneo (por que las glándulas paratiroides regulan el calcio); la hemorragia y las infecciones de la herida.
Tratamiento con yodo radiactivo
El tiroides absorbe casi todo el yodo de la sangre, por lo que el yodo radiactivo (I-131) puede destruir la glándula tiroides sin afectar al resto del organismo. Es el tratamiento recomendado como tratamiento complementario tras extirpar el tiroides y también cuando el cáncer de tiroides se ha propagado fuera del cuello a otras partes del cuerpo.
El I-131 puede utilizarse a dosis altas en algunos cánceres papilares o foliculares localizados.
Se administra de una vez en forma de cápsula; irradiando directamente el tejido tiroideo, destruyéndolo. A las pocas semanas el yodo radiactivo desaparece del cuerpo. Para que este tratamiento sea más eficaz, se suele suspender el tratamiento hormonal de hormona tiroidea 4 ó 5 semanas antes, aunque esto puede provocar un hipotiroidismo.
Los efectos secundarios de este tratamiento son escasos, en forma de molestias en el cuello y boca seca, y se recomienda que las mujeres en edad fértil eviten un embarazo dentro del primer año de este tratamiento.
Tras la cirugía del tiroides o su ablación con yodo radiactivo, suele ser necesaria la reposición de las hormonas tiroideas con la hormona sintética levotiroxina.
La hormona tiroidea también se debe utilizar como tratamiento ya que niveles altos de esta hormona disminuye los niveles de otra hormona TSH (hormona estimulante de tiroides); estos niveles bajos de TSH resultan eficaces para controlar el cáncer de tiroides.
Terapia Hormonal
Tras la cirugía del tiroides o su ablación con yodo radiactivo, suele ser necesaria la reposición de las hormonas tiroideas con la hormona sintética levotiroxina.
La hormona tiroidea también se debe utilizar como tratamiento ya que niveles altos de esta hormona disminuye los niveles de otra hormona TSH (hormona estimulante de tiroides); estos niveles bajos de TSH resultan eficaces para controlar el cáncer de tiroides.
Quimioterapia
La quimioterapia NO es muy eficaz contra el cáncer de tiroides, aunque, en ocasiones, es necesaria porque no han tenido éxito otros tratamientos. Hay diferentes fármacos en investigación para mejorar la eficacia de la quimioterapia..
Radioterapia
La radioterapia es el empleo de radiaciones ionizantes para el tratamiento, local o locorregional, de determinados tumores que emplea rayos X con altas dosis de irradiación.
Su objetivo es destruir las células tumorales causando el menor daño posible a los tejidos sanos que rodean dicho tumor.
Generalmente, este tipo de tratamiento no se usa contra cánceres que absorben yodo, porque en este caso se suelen tratar con yodo radioactivo. La radioterapia se utiliza en cánceres que no absorben yodo, después de la cirugía para aumentar el control local, o para tratar las recurrencias o paliar las metástasis.
La radioterapia puede producir como efectos secundarios, lesiones cutáneas similares a una quemadura por el sol.
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como la tráquea, la medula espinal, los pulmones, el corazón, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar. Los más empleados son una máscara de material termoplástico que se adapta al contorno del paciente.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..
-
V
- Vagina (Cáncer)
- Cáncer que se forma en los tejidos de la vagina (vía del parto). La vagina se extiende desde el cuello uterino (la abertura del útero) hasta el exterior del cuerpo.
El cáncer de vagina es un tumor muy poco común, representando entre el 1-2% de los cánceres ginecológicos.
Por lo general hay dos tipos de cáncer de vagina:- Carcinoma de células escamosas: cáncer que se origina en las células que forman la pared de la vagina. Es el más frecuente, y aparece en mujeres mayores de 60 años.
- Adenocarcinoma: cáncer que se origina en las glándulas de la vagina.
- Existen otros tipos de cáncer de vagina pero son realmente excepcionales, como por ejemplo melanoma o sarcoma de vagina.
Elección del tratamiento
Una vez que se ha confirmado el diagnóstico de cáncer de vagina y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado para curarla. El ginecólogo y/o el oncólogo le recomendará y explicará las posibilidades de tratamiento más adecuadas en su caso para que una vez que haya recibido la suficiente información pueda tomar una decisión.
Los tratamientos más frecuentemente empleados en el cáncer de vagina son la cirugía, la radioterapia, y la quimioterapia.
Este tratamiento puede variar en función de varios factores (estadio, tipo de tumor, la edad, el estado general del paciente) siendo el más importante el estadio del tumor:
Estadio 0 (carcinoma in situ)
El tratamiento para el estadio 0 puede incluir los siguientes procedimientos:
- Escisión local amplia, con un injerto de piel o sin este.
- Vaginectomía parcial o total, con injerto de piel o sin este.
- Quimioterapia tópica.
- Cirugía láser.
- Radioterapia interna.
Cáncer de vagina en estadio I
El tratamiento del cáncer de vagina de células escamosas en estadio I puede incluir los siguientes procedimientos:
- Radioterapia interna, con radioterapia externa o sin esta, dirigidas a los ganglios linfáticos o los tumores grandes.
- Escisión local amplia o vaginectomía con reconstrucción de la vagina. Se puede administrar radioterapia después de la cirugía.
- Vaginectomía y disección de ganglios linfáticos, con reconstrucción de la vagina o sin esta. Se puede administrar radioterapia después de la cirugía.
El tratamiento del adenocarcinoma vaginal en estadio I puede incluir los siguientes procedimientos:
- Vaginectomía, histerectomía y disección de ganglios linfáticos. Después de la cirugía, se puede hacer una reconstrucción de la vagina o administrarse radioterapia.
- Radioterapia interna, con radioterapia externa o sin esta, dirigidas a ganglios linfáticos.
- Combinación de tratamientos, que puede incluir escisión local amplia, con disección de ganglios linfáticos o sin esta, y radioterapia interna.
Cáncer de vagina en estadio II
El tratamiento del cáncer de vagina en estadio II es el mismo para el cáncer de células escamosas y el adenocarcinoma. Puede incluir los siguientes procedimientos:
- Radioterapia interna y externa dirigida a la vagina, con radioterapia externa dirigida a los ganglios linfáticos o sin ella.
- Vaginectomía o exenteración pélvica, con radioterapia o sin ella.
Cáncer de vagina en estadio III
El tratamiento del cáncer de vagina en estadio III es el mismo para el cáncer de células escamosas y el adenocarcinoma. El tratamiento puede incluir radioterapia interna y externa, con cirugía o sin esta.
Cáncer de vagina en estadio IVA
El tratamiento del cáncer de vagina en estadio IVA es el mismo para el cáncer de células escamosas y el adenocarcinoma. El tratamiento puede incluir radioterapia interna y externa, con cirugía o sin esta.
Cáncer de vagina en estadio IVB
El tratamiento del cáncer de vagina en estadio IVB es el mismo para el cáncer de células escamosas y el adenocarcinoma. El tratamiento puede incluir los siguientes procedimientos:
- Radioterapia como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
- También se puede administrar quimioterapia.
Opciones de tratamiento para el cáncer de vagina recidivante
El tratamiento del cáncer de vagina recidivante puede incluir los siguientes procedimientos:
- Exenteración pélvica.
- Radioterapia.
Cirugía
La mayoría de los tumores de vagina se diagnostican en fases tempranas, es decir, no se han diseminado fuera de la vagina, por lo que la cirugía suele ser el tratamiento más importante y el primero en llevarse a cabo en la mayoría de estos tumores.
En ocasiones, después de la cirugía puede ser necesaria la radioterapia para asegurarse que se eliminan todas las células malignas.
Las técnicas quirúrgicas para tratar el cáncer de vagina son:
- Cirugía con láser: se utiliza el láser como si fuera un bisturí para extirpar tumores superficiales.
- Escisión local amplia: similar a la anterior, pero realizada con bisturí extirpando el cáncer junto con parte del tejido sano que lo rodea.
- Vaginectomía: se extirpa el tumor con toda la vagina.
- Linfadenectomía: extirpación de los ganglios linfáticos que hay en la pelvis o en las ingles.
- Exenteración pélvica: es una cirugía de gran envergadura que se utiliza en casos extremos como por ejemplo cuando hay una recaída en la pelvis. Se extirpa la vagina, los ovarios, los ganglios linfáticos, el recto y la vejiga, y se realizan orificios artificiales para poder evacuar la orina y las heces.
QuimioterapiaLa quimioterapia es una de las modalidades terapéuticas más empleada en el tratamiento del cáncer, y consiste en la administración de medicamentos para detener el cáncer.
Sin embargo la quimioterapia no es un tratamiento habitual en el cáncer de vagina y sólo se emplea:
De forma tópica, en forma de pomada vaginal para eliminar células malignas. La quimioterapia tópica debe repetirse varias veces (alrededor de 10 veces) y puede ocasionar irritación de la vagina o de la vulva. Este tratamiento es poco habitual y sólo debe utilizarse en casos muy seleccionados.
De forma intravenosa para detener el crecimiento tumoral en estadios más avanzados.Radioterapia
La radioterapia es el empleo de radiaciones ionizantes para el tratamiento, local o locorregional, de determinados tumores que emplea rayos X con altas dosis de irradiación. Su objetivo es destruir las células tumorales causando el menor daño posible a los tejidos sanos que rodean dicho tumor.
En los tumores de vagina, la radioterapia que se aplica puede ser externa o interna, aunque generalmente se combinan ambas modalidades.
En la radioterapia externa se emplean equipos generadores de radiación (aceleradores lineales) que en ningún momento contactan con la paciente. La radioterapia interna consiste en la colocación de materiales radiactivos próximos a la zona tumoral. Se introducen en la vagina, por lo que se denomina radioterapia endocavitaria.
El tratamiento con radioterapia siempre es individualizado, es decir, cada enferma tendrá su tratamiento específico y distinto al de otra paciente.
Según la finalidad con que se emplee, la radioterapia puede ser curativa o paliativa para aliviar síntomas provocados por el cáncer como dolor, sangrado vaginal, etc.
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como la vejiga, el recto, las cabezas femorales, entre otras. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..
Radioterapia interna
Es una técnica de tratamiento que consiste en introducir en el interior del organismo isótopos radiactivos. Se pueden implantar de forma temporal o permanente en la zona a tratar.
Con la radioterapia interna se logra administrar altas dosis de radiación a cortas distancias, de tal forma, que llega muy poca dosis a los tejidos sanos circundantes al implante.
¿Cómo se colocan los implantes?
Dependiendo del tipo de implante que se vaya a realizar es necesario permanecer ingresado en el hospital durante 1 o dos días, en otros casos el paciente podrá irse a su casa el mismo día tras recibir el tratamiento. Bajo sedación o anestesia general, se efectuará la colocación de los isótopos radiactivos.
¿Es necesario permanecer aislado?
En ocasiones, mientras tenga colocados los implantes es necesario que permanezca en una habitación, preparada especialmente para tal fin.
El paciente estará controlado, en todo momento, a través de un monitor de televisión por el personal sanitario responsable de su cuidado.¿Cuánto dura el tratamiento?
La duración del tratamiento dependerá en gran medida del tipo de isótopo que se haya empleado en el implante y de la cantidad de dosis que se quiera administrar en la zona del tumor, pero generalmente oscila entre minutos y días.
- Vejiga (Cáncer)
Cáncer que se forma en los tejidos de la vejiga (el órgano que almacena orina). La mayoría de los cánceres de vejiga son carcinomas de células de transición (cáncer que empieza en células que normalmente forman el recubrimiento interno de la vejiga).
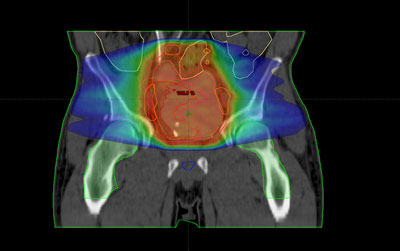
Otros tipos incluyen el carcinoma de células escamosas (cáncer que empieza en células delgadas y planas) y el adenocarcinoma (cáncer que empieza en las células que elaboran y liberan moco y otros líquidos). Las células que forman el carcinoma de células escamosas y el adenocarcinoma se desarrollan en el recubrimiento interno de la vejiga como resultado de irritación crónica e inflamación.
Carcinoma de células transicionales: es el tipo de cáncer más frecuente en la vejiga. Supone aproximadamente el 90% de todos los tumores en esta localización.
Una variedad de carcinoma de células transicionales es el papilar, que crece hacia el interior de la vejiga en forma de dedo o seta. Es un tumor de buen pronóstico.
Cuando el tumor está únicamente localizado en la capa más interna de la vejiga sin invadir otras capas más profundas de la pared, se le denomina carcinoma no invasivo o no infiltrante. Cuando el tumor invade la capa muscular de la pared vesical se le denomina invasivo o infiltrante.
Carcinoma escamoso: supone tan sólo un 2% del total de tumores de vejiga.
Adenocarcinoma: entre un 1 y un 2% de todos los tumores de vejiga son adenocarcinomas.Elección del tratamiento
Una vez que se ha confirmado el diagnóstico de cáncer de vejiga y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado. El especialista le recomendará y explicará las posibilidades más adecuadas en su caso, para que una vez que haya recibido la suficiente información pueda, junto con su médico tomar una decisión.
El tratamiento del cáncer de vejiga, como ocurre en la mayoría de los tumores, es un tratamiento multidisciplinar. Distintas especialidades trabajan juntas para combinar terapias y ofrecer al paciente las mayores posibilidades de curación.
El plan de tratamiento del cáncer de vejiga se basa en una serie de normas y pautas (protocolo), establecidas por cada hospital basándose en la experiencia clínica.
Estos protocolos, recogen las indicaciones o limitaciones de tratamiento en función de una serie de factores:
- Tipo de cáncer.
- Estadio en el que se encuentra la enfermedad (TNM).
- Grado celular.
Probablemente, el médico también tendrá en cuenta, si además del cáncer de vejiga, existen otras enfermedades importantes que puedan dificultar la realización de algún tratamiento específico.
Por tanto el tratamiento propuesto por el especialista no va a ser el mismo en todos los pacientes.
Los tratamientos más frecuentemente empleados en el cáncer de vejiga son, fundamentalmente, la cirugía, la radioterapia, la inmunoterapia y la quimioterapia.
Cáncer de la vejiga en estadio 0 (carcinoma papilar y carcinoma in situ)El tratamiento para el estadio 0 puede incluir los siguientes procedimientos:
- Resección transuretral con fulguración.
- Resección transuretral con fulguración, seguida de terapia biológica intravesical o quimioterapia.
- Cistectomía segmentaria.
- Cistectomía radical.
Cáncer de la vejiga en estadio IEl tratamiento del cáncer de vejiga en estadio I puede incluir los siguientes procedimientos:
- Resección transuretral con fulguración.
- Resección transuretral con fulguración seguida por terapia biológica intravesical o quimioterapia.
- Cistectomía segmentaria o radical.
- Radioterapia con implantes con o sin radioterapia externa.
Cáncer de la vejiga en estadio IIEl tratamiento del cáncer de vejiga en estadio II puede incluir los siguientes procedimientos:
- Cistectomía radical con cirugía para extirpar los ganglios linfáticos de la pelvis o sin esta.
- Quimioterapia de combinación seguida de cistectomía radical.
- Radioterapia externa junto con quimioterapia.
- Radioterapia con implantes antes o después de la radioterapia externa.
- Resección transuretral con fulguración.
- Cistectomía segmentaria.
Cáncer de la vejiga en estadio IIIEl tratamiento del cáncer de vejiga en estadio III puede incluir los siguientes procedimientos:
- Cistectomía radical, con cirugía o sin esta, para extirpar los ganglios linfáticos de la pelvis.
- Quimioterapia de combinación seguida de cistectomía radical.
- Radioterapia externa combinada con quimioterapia.
- Radioterapia externa con radioterapia con implantes.
- Cistectomía segmentaria.
Cáncer de la vejiga en estadio IV
El tratamiento del cáncer de vejiga en estadio IV puede incluir los siguientes procedimientos:
- Cistectomía radical, con cirugía o sin esta, para extirpar los ganglios linfáticos de la pelvis.
- Radioterapia externa (puede ser como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida).
- Derivación de la orina como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
- Cistectomía como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
- Quimioterapia sola o después del tratamiento local (cirugía o radioterapia).
Opciones de tratamiento para el cáncer de vejiga recidivante
El tratamiento del cáncer de vejiga recidivante depende del tratamiento anterior y el lugar donde el cáncer recidivó. El tratamiento puede incluir los siguientes procedimientos:
- Cirugía.
- Quimioterapia.
- Radioterapia.
Cirugía
El tipo de cirugía que se puede aplicar en el cáncer de vejiga varía en función del estadio en el que se encuentra el tumor.
Cuando el cáncer de vejiga es un tumor superficial es posible realizar una resección transuretral (RTU) del mismo. Se realiza empleando un aparato denominado resector, que se introduce en la vejiga a través de la uretra. Consiste en la resección y extracción de pequeños fragmentos de tejido vesical.
Si la lesión de la vejiga es infiltrante una RTU no suele ser suficiente para extirpar por completo el tumor, por lo que es preciso realizar una cirugía más amplia que consiste en la extirpación parcial o completa de la vejiga. A este tipo de cirugía se le denomina cistectomía parcial o radical, respectivamente.
La cistectomía radical es la técnica más empleada. Además de la extirpación de la vejiga es preciso una resección de los ganglios linfáticos próximos y de los órganos vecinos. En el hombre se extrae la próstata y vesículas seminales y en la mujer el útero, ovarios y parte de la vagina.Quimioterapia
La quimioterapia es un tratamiento del cáncer que utiliza medicamentos para interrumpir el crecimiento de células cancerosas, mediante su destrucción o evitando su multiplicación. Cuando la quimioterapia se administra por boca o se inyecta en una vena o músculo, los medicamentos ingresan en el torrente sanguíneo y pueden llegar a las células cancerosas en todo el cuerpo (quimioterapia sistémica).
Cuando la quimioterapia se coloca directamente en la columna vertebral, un órgano o una cavidad corporal como el abdomen los medicamentos afectan principalmente las células cancerosas de esas áreas (quimioterapia regional). El cáncer de vejiga se puede tratar con quimioterapia intravesical (entra en la vejiga mediante un tubo introducido en la uretra). La forma de administración de la quimioterapia depende del tipo y el estadio del cáncer que está siendo tratado.
Radioterapia
Su objetivo es destruir las células tumorales causando el menor daño posible a los tejidos sanos que rodean dicho tumor.
La radioterapia se puede emplear como tratamiento único en aquellos pacientes en los que no se ha podido realizar una cirugía, por lo avanzado de la enfermedad o por su estado general.
Asimismo, se puede administrar antes de la cirugía para disminuir su tamaño y facilitar la extirpación del tumor, o después de la misma, para destruir las posibles células tumorales que hayan podido quedar tras la intervención.
En casos muy seleccionados, la radioterapia se puede administrar con o sin quimioterapia, tras una resección transuretral, con el objetivo de destruir el tumor y evitar una cistectomía.
El tratamiento con radioterapia siempre es individualizado, es decir, cada enfermo tendrá su tratamiento específico y distinto al de otro paciente, dependiendo de la extensión de la enfermedad.
La radioterapia para el cáncer de vejiga puede ser de 2 tipos:
- Externa: se emplean máquinas de gran tamaño que, en ningún momento contactan con el enfermo.
- Interna: también denominada radioterapia intersticial. Se utiliza material radiactivo que se introduce en el interior del organismo en contacto directo con el tumor.
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como las cabeas femorales, el recto, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..Radioterapia Interna
Es una técnica de tratamiento que consiste en introducir en el interior del organismo isótopos radiactivos. Se pueden implantar de forma temporal o permanente en la zona a tratar.
Con la radioterapia interna se logra administrar altas dosis de radiación a cortas distancias, de tal forma, que llega muy poca dosis a los tejidos sanos circundantes al implante.
¿Cómo se colocan los implantes?Dependiendo del tipo de implante que se vaya a realizar es necesario permanecer ingresado en el hospital durante 1 o dos días, en otros casos el paciente podrá irse a su casa el mismo día tras recibir el tratamiento. Bajo sedación o anestesia general, se efectuará la colocación de los isótopos radiactivos.
¿Es necesario permanecer aislado?
En ocasiones, mientras tenga colocados los implantes es necesario que permanezca en una habitación, preparada especialmente para tal fin.
El paciente estará controlado, en todo momento, a través de un monitor de televisión por el personal sanitario responsable de su cuidado.¿Cuánto dura el tratamiento?
La duración del tratamiento dependerá en gran medida del tipo de isótopo que se haya empleado en el implante y de la cantidad de dosis que se quiera administrar en la zona del tumor, pero generalmente oscila entre minutos y días.
- Vesícula Biliar (Cáncer)
- Cáncer que se forma en tejidos de la vesícula biliar. La vesícula biliar es un órgano en forma de pera, que se encuentra debajo del hígado, que recolecta y almacena la bilis (líquido elaborado por el hígado para digerir las grasas). El cáncer de vesícula biliar comienza en la capa interna de tejido y se disemina a través de las capas externas mientras crece.
El carcinoma de la vesícula biliar es un tumor relativamente raro, suponiendo el 5º de los tumores gastrointestinales.
La mayoría de los carcinomas de la vesícula biliar son adenocarcinomas. Son raros otros tipos histológicos de tumores como los de células pequeñas indiferenciados, escamosos, sarcomas o incluso linfomas.
El factor pronóstico más importante es el grado de extensión del tumor, según la clasificación en estadios que se ha descrito en el apartado anterior. Así un tumor en estadio I puede curarse, mientras que la supervivencia a los 5 años en el estadio II es ya inferior al 10% y prácticamente nula en el estadio IV.
La edad, el estado de salud general de la persona, así como los síntomas que padece, también pueden influir en el pronóstico de este tumor.
Opciones de TratamientoCáncer de la vesícula biliar localizado
El tratamiento del cáncer de vesícula biliar localizado puede incluir los siguientes procedimientos:
- Cirugía para extirpar la vesícula biliar y parte del tejido que la rodea. También se pueden extirpar el hígado y los ganglios linfáticos cercanos. Después de la cirugía se puede administrar radioterapia, con quimioterapia o sin esta.
- Radioterapia, con quimioterapia o sin ella.
Cáncer de la vesícula biliar inoperableEl tratamiento del cáncer de vesícula biliar inoperable puede incluir los siguientes procedimientos:
- Radioterapia como tratamiento paliativo, con cirugía o sin esta, o la colocación de cánulas, para aliviar los síntomas causados por el bloqueo de los conductos biliares.
- Cirugía como tratamiento paliativo para aliviar los síntomas causados por el bloqueo de los conductos biliares.
- Quimioterapia como tratamiento paliativo para aliviar los síntomas causados por el cáncer.
Cirugía
El tumor en estadio I, localizado en la vesícula biliar, es resecable quirúrgicamente, si el paciente se encuentra en condiciones físicas para someterse a esta intervención. Este es el único estadio en el que el tumor puede ser curable mediante la extirpación quirúrgica. Pero desafortunadamente esta situación solo supone del 10 al 30% de los casos.
La cirugía consiste en una colecistectomía, una extirpación de la vesícula biliar y de los tejidos que la rodean (conducto biliar extrahepático, y tejido hepático adyacente), así como de los ganglios linfáticos de la zona.
Cuando el tumor sobrepasa estos límites e infiltra los tejidos de órganos vecinos, como el hígado, páncreas, intestino delgado o vasos sanguíneos, la extirpación quirúrgica del tumor puede ser posible, aunque muy dificultosa y con mucha probabilidad de complicaciones postquirúrgicas, pero también puede ser imposible resecar el tumor por completo. En estas circunstancias el tratamiento quirúrgico puede tener un objetivo paliativo solamente, para liberar la obstrucción de la bilis, mediante una derivación quirúrgica de la vía biliar o para colocación de un implante endoscópico.Quimioterapia
La quimioterapia puede administrarse en concomitancia con la radioterapia en la enfermedad localmente avanzada. En esta situación el fármaco más utilizado y estudiado es el 5-Fluorouracilo.
Cuando la enfermedad está avanzada el tratamiento tiene solamente un objetivo paliativo.
El cáncer de la vesícula biliar se considera como un tumor particularmente quimio-resistente. Han sido pocos lo fármacos estudiados en el tratamiento de esta enfermedad en fase avanzada. Se utilizan esquemas de poliquimioterapia con el 5-Fluoruracilo como fármaco principal, asociado a platinos (Cisplatino, Oxaliplatino) y, más recientemente también a la Gemcitabina. La posibilidades de respuesta a estos fármacos es baja. La mediana de supervivencia no llega al año.Radioterapia
El carcinoma de la vesícula biliar tiene un patrón de diseminación locorregional por lo que un tratamiento local como la radioterapia puede tener un papel importante en esta enfermedad.
Cuando el tumor sobrepasa los límites de la vesícula biliar o es irresecable la radioterapia puede administrarse como tratamiento paliativo.
Actualmente se contempla también que la radioterapia puede mejorar las posibilidades de control local de la enfermedad tras una cirugía completa en enfermedad locálmente avanzada, pero este enfoque terapéutico aun está bajo investigación mediante ensayos clínicos.
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como la medula espinal, el hígado, el estomago, el páncreas, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..
.png)
